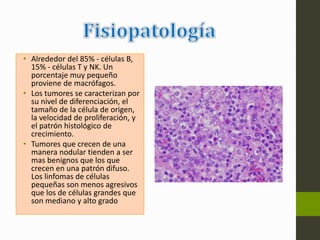
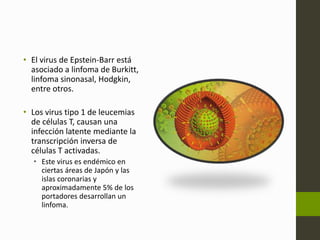
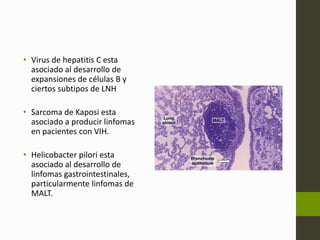
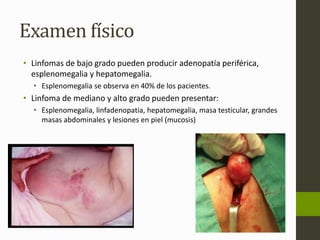
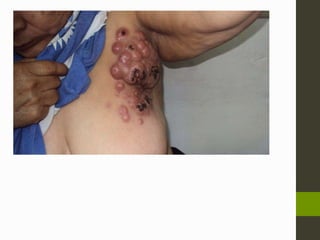
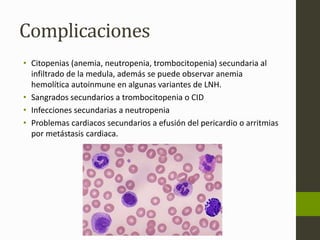
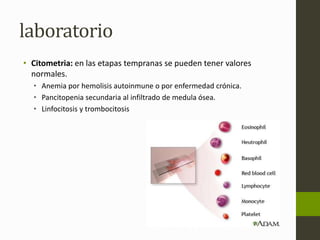
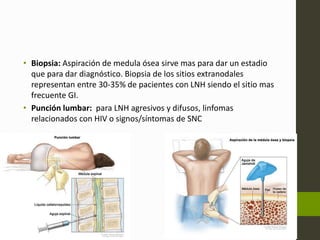
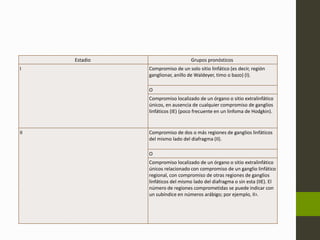
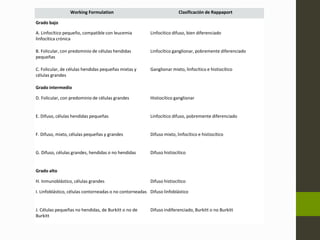
El linfoma no Hodgkin (LNH) son tumores malignos originados del tejido linfático que pueden ser causados por translocaciones cromosómicas, infecciones virales, factores ambientales, y estados de inmunodeficiencia. Existen varios subtipos de LNH que se clasifican según el tipo de célula afectada, su grado de diferenciación y patrón de crecimiento. El diagnóstico y tratamiento del LNH depende del estadio y grupo pronóstico determinado mediante biopsia y examen físico