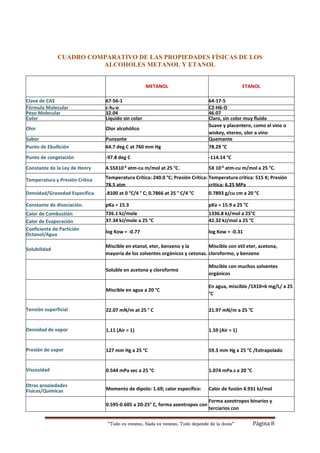
Este documento compara las propiedades físicas y químicas del metanol y el etanol, destacando que aunque se ven iguales, el metanol es extremadamente tóxico incluso en pequeñas dosis mientras que el etanol es seguro en cantidades moderadas. Incluye tablas comparativas de sus puntos de ebullición, solubilidad, densidad, y otras propiedades, así como ejemplos de reacciones como la oxidación y deshidratación para diferenciarlos.