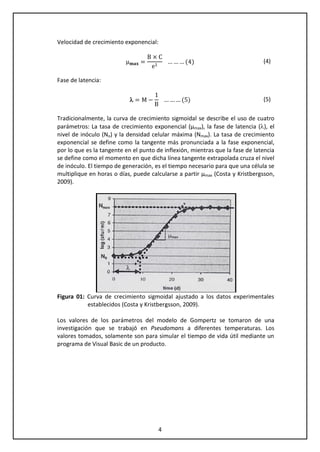
Este documento presenta un programa en Visual Basic para simular el crecimiento microbiano de Pseudomonas spp. en un concentrado de chicha morada almacenado a 20°C. El modelo de Gompertz modificado se utiliza para predecir que el nivel máximo de contaminación es de 8,7884 Log UFC/ml y que el tiempo de vida útil estimado del producto es de 88 horas. Los parámetros del modelo se obtienen de un estudio sobre el crecimiento de Pseudomonas spp. en carne de vacuno a diferentes temperaturas.