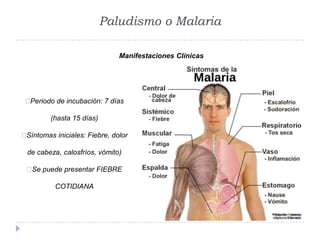
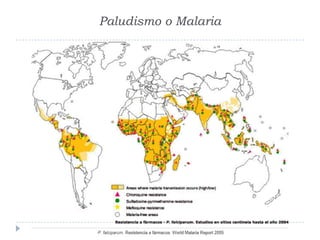
Este documento describe diferentes parásitos protozoarios que afectan a los humanos, incluyendo Trypanosoma cruzi que causa la enfermedad de Chagas, especies de Trypanosoma y Leishmania que causan diferentes enfermedades, y Plasmodium spp. que causan malaria. Explica sus ciclos de vida, síntomas, formas de transmisión, diagnóstico y tratamiento. Además, proporciona detalles epidemiológicos sobre la distribución de estas enfermedades.