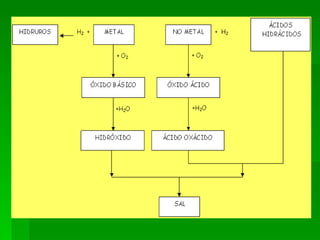
El documento describe diferentes tipos de óxidos, incluyendo óxidos básicos metálicos formados por la reacción de un metal con oxígeno, óxidos ácidos o anhídridos formados por la reacción de un no metal con oxígeno, óxidos neutros formados por la reacción de un no metal con oxígeno, óxidos anfóteros formados por la reacción de metales como cromo y manganeso con diferentes estados de oxidación con oxígeno, óxidos mixtos o salinos formados por