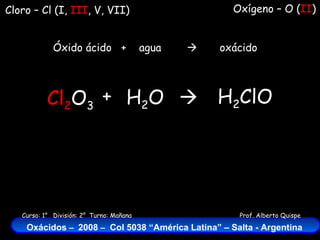
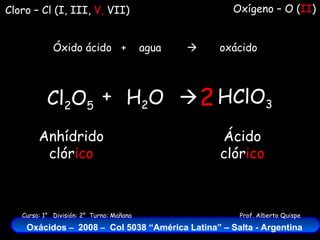
El documento describe las fórmulas, nombres y ecuaciones químicas de formación de los diferentes óxidos de cloro y sus correspondientes ácidos. Explica que el cloro puede tener valencias I, III, V y VII y que al reaccionar con oxígeno y agua forma ácidos como el ácido hipocloroso, el ácido cloroso, el ácido clórico y el ácido perclórico.