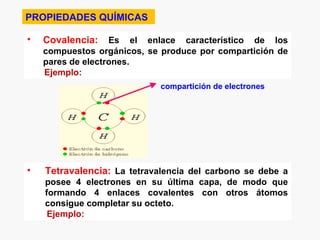
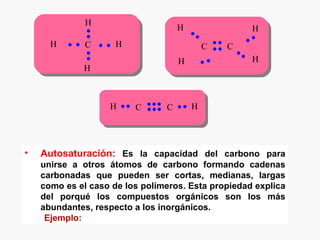
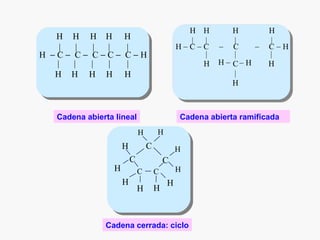
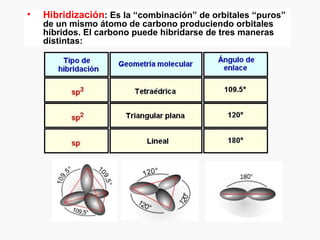
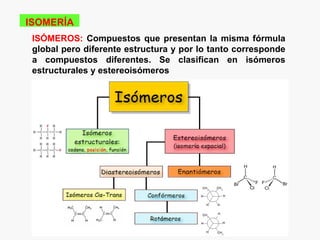
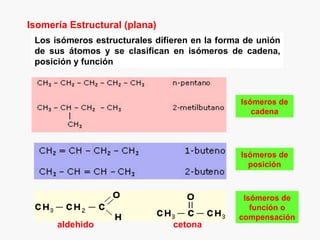
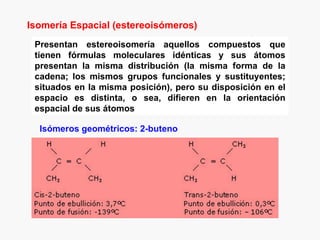
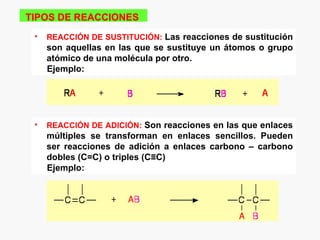
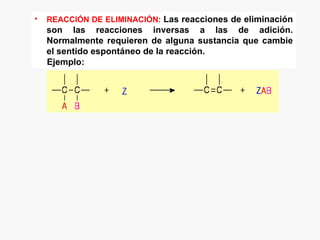
Este documento resume los conceptos básicos de la química orgánica, incluyendo que estudia los compuestos de carbono e hidrógeno, que forman las estructuras celulares de los seres vivos, y que incluye biomoléculas como proteínas y glúcidos. También describe las propiedades del carbono, los tipos de enlaces, isomería, y reacciones como sustitución, adición y eliminación.