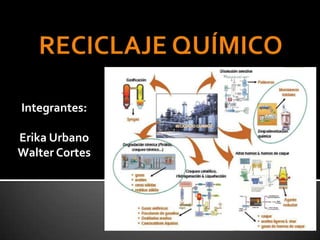
Reciclaje Quimico - EPN
- 2. El reciclaje mecánico se vuelve menos rentable por los materiales plásticos: muy degradados mezclados con todo tipo de sustancias que su separación y de limpieza complicada.
- 3. Alternativa de aprovechamiento son reacciones químicas. Los plásticos los más comunes entre los RSU son sólo seis, todos ellos termoplásticos: Polietileno Tereftalato (PET) – p.e. cintas de video y audio; películas radiográficas, Polietileno de Alta Densidad (PEAD, HDPE) – p.e. contenedores de basura, Polietileno de Baja Densidad (PEBD, LDPE) – p.e. envases de alimentos congelados, juguetes Cloruro de Polivinilo (PVC) – p.e. depósitos y cañerías de desagüe. Polipropileno (PP) – p.e. material de bisagras. Poliestireno (PS) – p.e. envases, tapaderas de bisutería, muebles de jardín
- 4. El RECICLADO QUÍMICO, denominado también reciclado terciario es un proceso por el que a partir de materiales de post consumo se llega a la obtención de los monómeros de partida u otros productos, como gas de síntesis y corrientes hidrocarbonadas, que serán transformados posteriormente en plásticos o bien en otros derivados.
- 5. El proceso químico seguido es diferente según haya sido el tipo de reacción de polimerización.
- 6. En el reciclado químico de los productos de adición no es imprescindible separar los plásticos según su naturaleza, ya que la mezcla de productos obtenidos en su proceso (compuestos aromáticos y alifáticos) puede utilizarse conjuntamente como alimentación en la industria petroquímica.
- 7. Craqueo y pirólisis térmica (carbonización a baja temperatura) Pueden ser solamente térmicos o también catalizados. Se realizan generalmente en ausencia de oxígeno a temperaturas entre 400 -800 ºC y a presión reducida. No arde, libera sus constituyentes petroquímicos produciendo: ▪ Gas de síntesis ▪ Fuel ▪ Ceniza
- 8. Craqueo y pirólisis térmica (carbonización a baja temperatura)
- 9. Gasificación El calentamiento por sobre los 700C en presencia de aire u oxígeno produce reacciones de oxidación Obtención de gas de síntesis, mezcla de CO2 y H2 La principal ventaja es la posibilidad de mezclar los distintos tipos de plásticos y la generación de hidrogeno que cada vez tiene mayor importancia.
- 10. Hidrogenación Es un proceso que licua los residuos plásticos antes de someterlos a tratamientos de pirólisis para conseguir olefinas y aromáticos. Tratamiento con hidrogeno y calor, las cadenas poliméricas son rotas y convertidas en un petróleo sintético que puede ser utilizado en refinerías o plantas químicas por la ausencia de oxigeno.
- 11. Tratamientos químicos, involucran reacciones de despolimerización o chemolisis que son aplicaciones de procesos solvolíticos Recupera los monómeros de partida que se destinan nuevamente a la obtención de polímero. Estos procesos pueden conseguir un nivel de reutilización del 90% Tal es el caso de los poliésteres, las poliamidas y poliuretanos, las reacciones de despolimerización. Así por ejemplo las tres reacciones más importantes que se aplican al PET son:
- 12. Hidrólisis Despolimerización total por acción del agua en presencia de ácidos o álcalis.
- 13. Metanólisis Es el proceso mas avanzado y complejo Capaz de quitar todos los colorantes e impurezas y es eficaz aun con residuos plásticos de baja calidad. Consigue la recuperación casi completa de los plásticos en términos de volumen y el producto final es resina virgen. Consiste en la despolimerización total del plástico por acción del metanol. Es un proceso de trans- esterificación en el que se obtiene tereftalato de metilo y etilenglicol.
- 14. Glicólisis Conduce a la despolimerización parcial por acción del etilenglicol, formando el éster hidroxietílico y mezcla de oligómeros. La mezcla de reacción se somete a purificación, siendo polimerizada posteriormente con resina virgen.
- 15. Debido al incremento en el uso vehicular miles de toneladas de llantas son generadas en todo el mundo. Se reporta que en países desarrollados una llanta es desechada por persona anualmente. La disposición final de las llantas usadas es el confinamiento en rellenos sanitarios a modo de pilas al aire libre, generando así problemas de salud y riesgo de incendio .
- 16. Los proceso aplicables a los neumáticos son: RECUPERACIÓN DE ENERGÍA POR INCINERACIÓN: valor calorífico de 33 MJ/kg, , sin embargo las emisiones producidas (dioxinas, furanos, etc.) no favorecen este proceso. GASIFICACIÓN PIRÓLISIS Los componentes principales de las llantas son: NR: caucho natural BR: Polibutadieno SBR: Estireno Butadieno. PLZ: Aditivos y plastificantes
- 17. GASES Y LIQUIDOS DE BAJA DENSIDAD que son útiles como combustibles. COQUE que contiene minerales TIPO DE NEGRO DE CARBÓN que puede ser tratado y convertido en carbón activo PIROLISIS PRODUCTOS descomposición térmica de macromoléculas en ausencia de oxígeno para la obtención de productos de menor peso molecular.
- 18. Para empezar con el proceso de Pirólisis es necesario fragmentar las llantas de desecho en trozos de 50X50 mm., para garantizar una apropiada reacción de pirolisis. Luego se transportan al reactor de pirolisis donde un catalizador de baja temperatura logra remover los azufres. A partir de la reacción completa y como consecuencia de ella se obtienen los siguientes componentes:
- 20. El proceso de pirólisis de llantas presenta tres etapas de descomposición térmica. El rango de temperatura se encuentra entre 120°C y 520°C. Las etapas correspondientes a: VOLATIZACIÓN DE PLASTIFICANTES. DEGRADACIÓN DEL CAUCHO NATURAL. DEGRADACIÓN DE CAUCHO SINTÉTICO.
