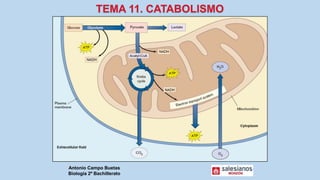
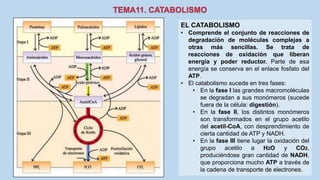
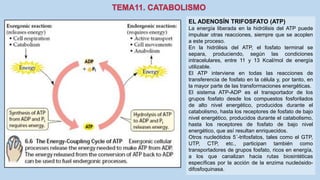
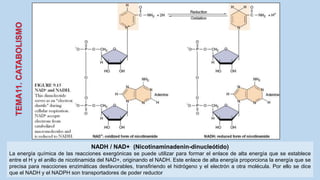
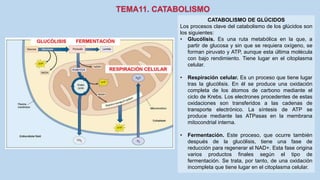
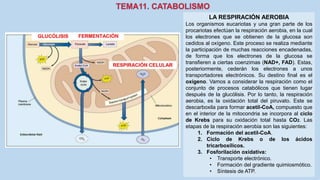
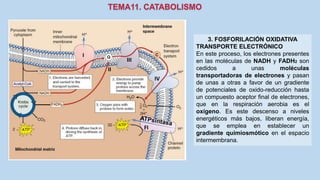
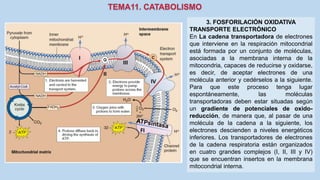
Este documento presenta un resumen de los principales procesos metabólicos que tienen lugar en las células, incluyendo la glucolisis, el ciclo de Krebs, la cadena de transporte de electrones y la fosforilación oxidativa. También describe brevemente la fermentación, el metabolismo en general, el papel del ATP como transportador de energía, y los transportadores de electrones como el NADH. El objetivo general del documento es proporcionar una visión de alto nivel de los procesos fundamentales del metabolismo celular.