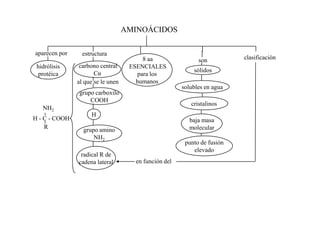
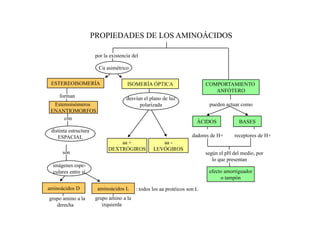
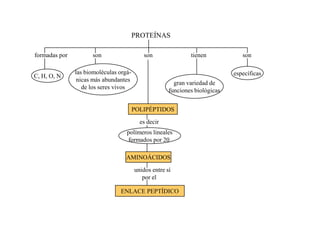
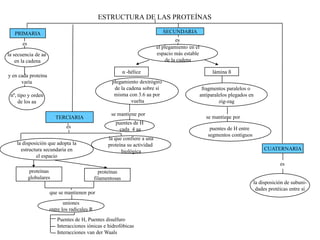
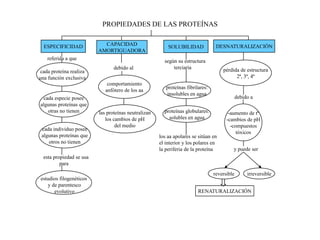
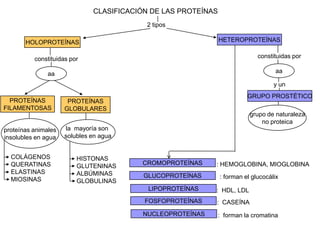
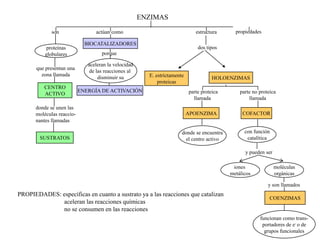
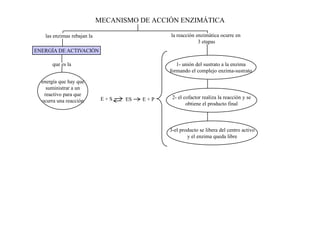
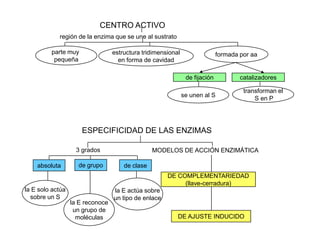
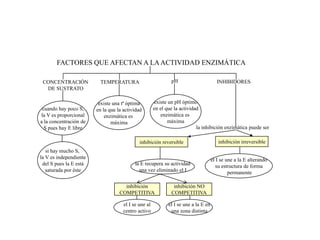
El documento resume las propiedades fundamentales de los aminoácidos, proteínas y enzimas. Los aminoácidos son los bloques de construcción de las proteínas y existen 20 tipos diferentes. Las proteínas adoptan estructuras primaria, secundaria, terciaria y cuaternaria y cumplen funciones estructurales, enzimáticas y otras en los seres vivos. Las enzimas son proteínas globulares que actúan como catalizadores biológicos acelerando las reacciones químicas a través de su centro activo.