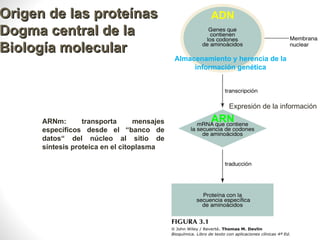
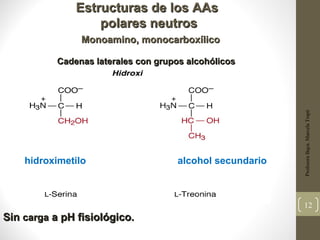
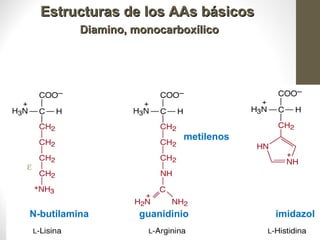
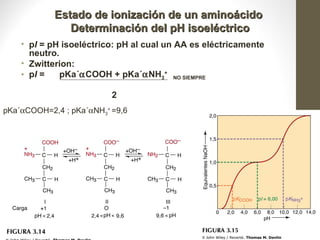
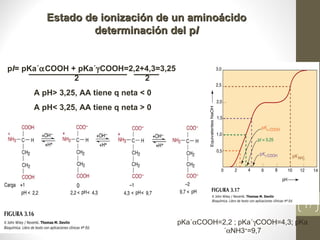
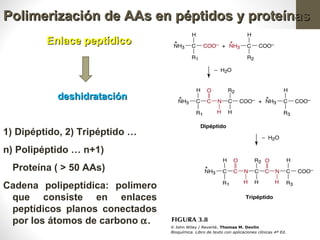
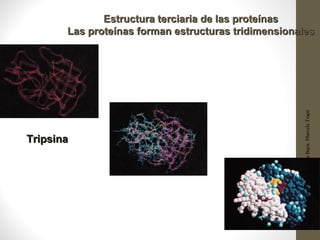
Este documento presenta una introducción a las proteínas. Explica que las proteínas son polímeros formados por la unión de 20 aminoácidos diferentes. Detalla las estructuras primarias, secundarias, terciarias y cuaternarias de las proteínas, y cómo estas estructuras determinan su función. Finalmente, clasifica las proteínas en globulares, fibrosas y otras categorías, dando ejemplos de cada tipo.