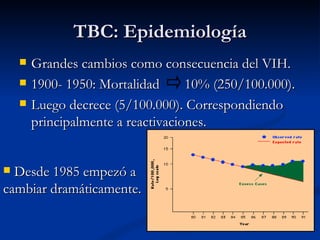
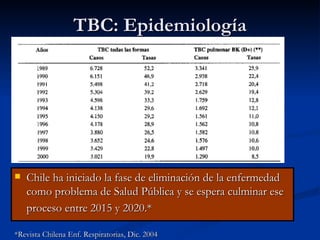
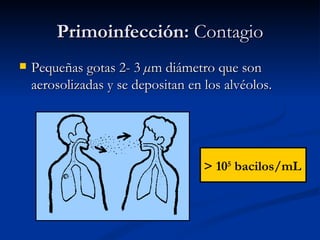
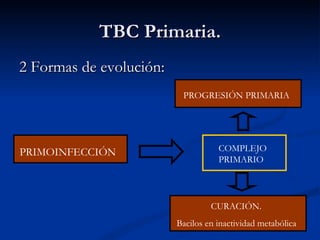
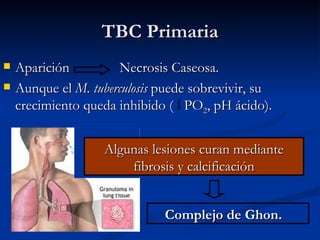
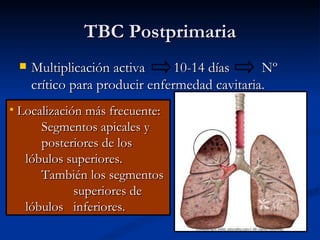
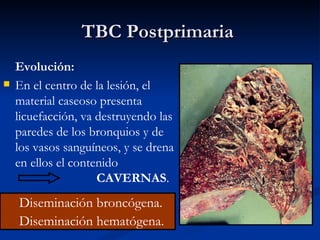
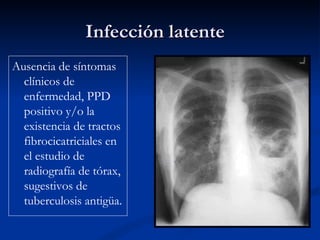
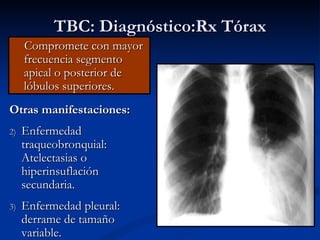
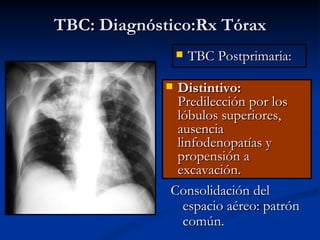
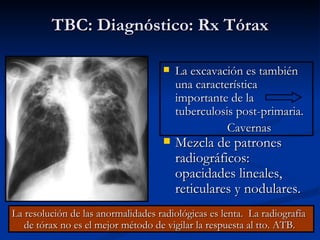
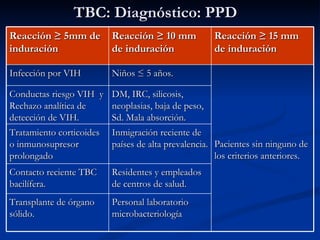
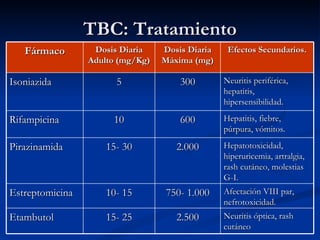
Este documento describe la tuberculosis pulmonar, definiéndola como una enfermedad infecciosa crónica causada por la inhalación del bacilo Mycobacterium tuberculosis. Explica que la tuberculosis puede presentarse como una infección primaria asintomática o como una reactivación de una infección latente, y que factores como el VIH aumentan el riesgo de reactivación. También resume los métodos de diagnóstico como la baciloscopía, la radiografía de tórax y la prueba cutánea de la tuberculina.