IRA Causas Tratamiento
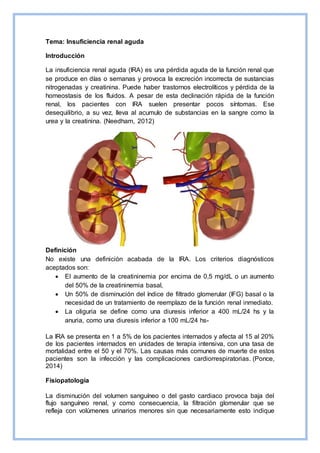
- 1. Tema: Insuficiencia renal aguda Introducción La insuficiencia renal aguda (IRA) es una pérdida aguda de la función renal que se produce en días o semanas y provoca la excreción incorrecta de sustancias nitrogenadas y creatinina. Puede haber trastornos electrolíticos y pérdida de la homeostasis de los fluidos. A pesar de esta declinación rápida de la función renal, los pacientes con IRA suelen presentar pocos síntomas. Ese desequilibrio, a su vez, lleva al acumulo de substancias en la sangre como la urea y la creatinina. (Needham, 2012) Definición No existe una definición acabada de la IRA. Los criterios diagnósticos aceptados son: El aumento de la creatininemia por encima de 0,5 mg/dL o un aumento del 50% de la creatininemia basal, Un 50% de disminución del índice de filtrado glomerular (IFG) basal o la necesidad de un tratamiento de reemplazo de la función renal inmediato. La oliguria se define como una diuresis inferior a 400 mL/24 hs y la anuria, como una diuresis inferior a 100 mL/24 hs- La IRA se presenta en 1 a 5% de los pacientes internados y afecta al 15 al 20% de los pacientes internados en unidades de terapia intensiva, con una tasa de mortalidad entre el 50 y el 70%. Las causas más comunes de muerte de estos pacientes son la infección y las complicaciones cardiorrespiratorias. (Ponce, 2014) Fisiopatología La disminución del volumen sanguíneo o del gasto cardiaco provoca baja del flujo sanguíneo renal, y como consecuencia, la filtración glomerular que se refleja con volúmenes urinarios menores sin que necesariamente esto indique
- 2. que el paciente tenga insuficiencia renal aguda (IRA), sino que tiene la llamada disfunción renal, insuficiencia prerrenal o insuficiencia renal fisiológica. La hipovolemia genera una caída en la presión arterial media, la cual es detectada por barorreceptores cardiacos y carotídeos cuya activación genera una serie de respuestas neuronales y humorales que se caracterizan por la estimulación del sistema nervioso simpático, del sistema renina-angiotensina- aldosterona y liberación de la hormona antidiurética. La adrenalina, la noradrenalina, la angiotensina II y la hormona antidiurética estimulan la vasoconstricción de lechos vasculares no esenciales como la circulación esplácnica y musculocutánea en su intento por mantener la presión sanguínea y preservar la perfusión cardiaca y cerebral. También disminuyen la pérdida de sodio y agua mediante la inhibición de las glándulas sudoríparas; como consecuencia de la hipoperfusión disminuye la presión de perfusión renal; sin embargo, la perfusión glomerular, la presión de ultrafiltrado y la tasa de filtración se preservan debido a la presencia de receptores en las arteriolas aferentes que se activan en respuesta a la reducción de la presión intraglomerular. Esta respuesta se caracteriza por vasodilatación de la arteriola aferente debido a un reflejo miogénico local. Otro mecanismo que genera dilatación de la arteria aferente es la síntesis de prostaglandinas vasodilatadoras, principalmente la prostaglandina E2 y la prostaciclina. La dilatación máxima de la arteriola aferente se da con una presión arterial media de 80 mmHg, por lo tanto, cifras menores a dicho valor se asocian a disminución crítica de la presión de ultrafiltrado glomerular y de la tasa de filtrado glomerular. La angiotensina II induce la constricción de la arteriola eferente. (Gainza, 2015) Clasificación por la etiología IRA pre-renales IRA renal o intrínseca IRA post-renal u obstructiva IRA Pre-renales Estas causas son comunes, siendo la principal la depleción del volumen intravascular. La fiebre, los vómitos y la diarrea pueden disminuir la perfusión renal. La deshidratación producida por cualquier causa, incluyendo los diuréticos, puede precipitar la IRA. La uremia prerrenal ocurre en las enfermedades que provocar una disminución del volumen efectivo de la sangre arterial. Estas enfermedades son la insuficiencia cardiaca, la insuficiencia hepática y el síndrome nefrótico. Los antiinflamatorios no esteroides (AINE) y los inhibidores de la enzima convertidora de angiotensina (IECA) son causas conocidas de uremia prerrenal. Los AINE afectan el riñón mediante el bloqueo de la ciclooxigenasa, provocando un aumento del tromboxano A2, un vasoconstrictor potente de las
- 3. arteriolas preglomerulares. Debido a que estos vasos aferentes son los que aportan la sangre al riñón, la vasoconstricción ocasiona una disminución de la perfusión glomerular. Los IECA bloquean la producción de angiotensina II, causando vasodilatación de las arteriolas eferentes posglomerulares, lo cual provoca una disminución de la presión glomerular, causante de aumento de la urea en sangre. La enfermedad de los grandes vasos, como la trombosis, la embolia y la disección, también pueden reducir la perfusión renal. (Needham, 2012) IRA renal o intrínseca Las causas renales de IRA se clasifican en tubular, glomerular, intersticial y vascular. Las causas más frecuentes de lesión tubular son la isquemia o la acción de nefrotoxinas. Si la uremia prerrenal y la mala perfusión continúan sin tratamiento, comienza a producirse la muerte de las células tubulares, condición conocida como “necrosis tubular aguda” (NTA). La necrosis tubular aguda no es una entidad aparte sino que es un marcador de un insulto isquémico mayor a los riñones. Por lo tanto, la uremia prerrenal y la isquemia tubular representan estadios en la progresión de la lesión tubular. La NTA presenta tres fases: iniciación, mantenimiento y recuperación. Luego de la injuria renal inicial, la fase de mantenimiento dura una a dos semanas. Durante la fase de recuperación, puede haber una poliuria y un retorno lento de la función renal. Hasta el momento, dicen los autores, no existe tratamiento que acelera la recuperación de la NTA. En los pacientes de alto riesgo es muy importante evitar el desarrollo de la NTA. Las enfermedades que aumentan el riesgo de NTA son la uremia prerrenal no tratada y el uso de fármacos nefrotóxicos, o la exposición a otras nefrotoxinas. La glomerulonefritis, una causa frecuente de IRA tiene manifestaciones sistémicas como la fiebre, la erupción y la artritis. La orina presenta cilindros hemáticos, hematuria y proteinuria. En todos los pacientes con glomerulonefritis es importante evaluar la presencia de enfermedades como el lupus eritematoso sistémico. En casos determinados puede ser necesaria la biopsia renal. La nefritis intersticial aguda es un trastorno intersticial que lleva a la IRA. Suele ser la consecuencia de una reacción alérgica. Los síntomas son la fiebre y la erupción. Puede haber eosinofilia y eosinófilos en orina. Las enfermedades autoinmunes, la infección y las enfermedades infiltrantes pueden provocar nefritis intersticial. Ante la sospecha de que la etiología puede ser un fármaco, se debe suspender inmediatamente su administración e indicar tratamiento de sostén. Los corticosteroides pueden ser útiles. (Ponce, 2014) Causas postrenales Las causas postrenales de IRA son consecuencia de la obstrucción en el tracto urinario. Entre ellas se encuentra la hipertrofia prostática, los catéteres, los
- 4. tumores, las estrecheses y los cristales. La vejiga neurogénica también puede provocar obstrucción. Debido a que las causas posrenales son reversible, su diagnóstico es muy importante. La recuperación de la función renal es directamente proporcional a la duración de la obstrucción. La ecografía renal es útil para detectar la hidronefrosis, con la ventaja de no requerir medio de contraste radiológico que pueda alterar la función renal.
- 5. Cuadro clínico de la insuficiencia renal aguda Las diversas formas de presentación de la IRA tienen diferentes signos y síntomas dependiendo de la causa desencadenante, y es hasta las 48 o 72 horas que se inician las manifestaciones de la falla renal propiamente dicha que son secundarios a la retención de productos nitrogenados, al desequilibrio hidroelectrolítico y alteraciones del equilibrio ácido-base. Diagnóstico de la insuficiencia renal aguda El diagnóstico de insuficiencia renal aguda se ha tratado de efectuar con las clasificaciones de RI-FLE, Akin y la cinética, las cuales se basan en la retención azoada y los volúmenes urinarios, lo que puede dar falsos positivos, falsos negativos y lo que es más peligroso, retardar el tratamiento de la IRA, ya que no se toma en cuenta que la hipovolemia, la disminución del gasto cardiaco y las otras causas que pueden producir injuria renal pueden dar disminución de los volúmenes urinarios y discreta retención azoada sin modificar la filtración glomerular ni los mecanismos de concentración y reabsorción tubular y lo único que provoca es una disfunción renal o la llamada insuficiencia renal funcional por mecanismos compensatorios, lo que me permitió realizar algunas modificaciones a estas clasificaciones para evitar lo antes referido . El diagnóstico de IRA se efectúa con base en cuatro puntos: 1. Causa o riesgo que provoca una injuria. 2. Alteraciones del flujo urinario en disminución o en aumento ya que debe recordarse que puede existir IRA de gasto alto. 3. Alteraciones de las pruebas funcionales renales o determinación de marcadores. 4. Biopsia renal percutánea, cuya indicación médica se debe de efectuar cuando exista oliguria o anuria de más de cuatro semanas, o en trabajos de investigación aprobados por los comités de ética y de investigación.
- 6. Tratamiento de la insuficiencia renal aguda El tratamiento ideal de la IRA es el dialítico y el médico en la actualidad no tiene ninguna aplicación en los países con capacidad científica adecuada. Pero éste se sigue utilizando en los países subdesarrollados que no cuentan con el personal capacitado y con los equipos de diálisis adecuados. El otro problema es el que para establecer la terapia de reemplazo renal tratan de cumplir los criterios de Acute Dialysis Quality Initiative(ADQI) que son los siguientes: Oliguria o anuria menor de 200 mL en 12 horas. Acidosis metabólica grave, con pH menor de 7.1. Hiperazotemia grave con BUN igual o mayor de 80 mg/dL. Hipercalemia igual o mayor de 6.5 mEq/L. Signos clínicos de toxicidad urémica. Hiponatremia o hipernatremia grave con Na menor de 115 o mayor de 160 mEq/L. Hipertermia. Anasarca o sobrecarga de líquidos importante. Insuficiencia orgánica múltiple que incluye la renal. (Needham, 2012) Tipos de terapia de reemplazo renal Hay varios tipos básicos de terapias de reemplazo renal, que son: diálisis peritoneal (DP), hemodiálisis intermitente (HI), terapia de reemplazo renal continúo (TRRC) y plasmaféresis (PM). En muchos hospitales la DP Y HI continúan siendo la modalidad más frecuentemente utilizada y en otros se utilizan las TRRC y la PM. Sin embargo, la mortalidad sigue siendo muy alta debido a que se utiliza en forma tardía o siguiendo las instrucciones de la ADQI o las clasificaciones de RIFLE, Akin y la cinética. Un buen nefrólogo o intensivista que maneje todas estas modalidades de diálisis y que conozca el momento idóneo de su aplicación, los riesgos de cada uno de ellos y los beneficios de cada procedimiento de acuerdo con la patología desencadenante de la IRA, obtendrá mayores beneficios al disminuir la morbilidad y mortalidad de este síndrome y esto se logra al efectuar un diagnóstico temprano que se basa en una depuración de creatinina endógena con orina de una, dos, tres, seis y hasta 24 horas menor de 15mL/min, U/PmOsm menor de 1 y Beta 2 microglobulina de 7.4mg/L sin importar los volúmenes urinarios del paciente ni la retención azoada y si existe inestabilidad hemodinámica del paciente la debe de mantener con sustancias vasoactivas, volumen, inotrópicos y monitoreo no invasivo por medio de bioimpedancia, lo cual mide todos los parámetros que permiten una homeostasis adecuada para lograr un éxito en la terapia. (Ponce, 2014)
- 7. Acetilcisteína para prevenir falla renal por medio de contraste El uso de acetilcisteína junto con hidratación en pacientes con falla renal crónica disminuye a más de la mitad la incidencia de deterioro de la función renal a las 48 horas (NNT = 10). La N-acetilcisteína (NAC) es un potente antioxidante que elimina una amplia gama de radicales libres derivados del oxígeno y podría ser capaz de prevenir el DRA-IC, a través de una mejora de la hemodinámica renal y de una reducción de la lesión tisular oxidativa directa. Se han publicado numerosos estudios sobre el efecto profiláctico de la NAC, con resultados contradictorios. Varios ensayos prospectivos y aleatorizados de pequeño tamaño han indicado que la administración de NAC junto con la hidratación redujo de manera significativa el DRA-IC en pacientes en alto riesgo, mientras que otros ensayos no han mostrado ningún beneficio adicional. El estudio aleatorizado más amplio hasta el momento (487 pacientes) que ha evaluado la eficacia de NAC en la prevención de Insuficiencia renal Aguda ha sido el realizado por Webb et al. La administración intravenosa de 500 mg de NAC inmediatamente antes de la intervención no aportó una protección renal a los pacientes con un deterioro de la función renal en comparación con placebo. La discrepancia entre estos estudios puede explicarse por el uso de técnicas, tipos y volúmenes de medios de contraste, momentos de uso, dosis de NAC y vías de administración (oral o intravenosa) diferentes. En algunos estudios, las tasas de disfunción renal descritas fueron muy superiores a las esperadas, y ello motivó la aparición de resultados estadísticamente significativos en grupos de pacientes relativamente pequeños. (Mehran, 2012) Tratamiento no dialitico Tratamiento Específico de las causas potencialmente reversibles IRA Prerrenal En estos casos es preciso diagnosticar y corregir las situaciones de deplección de volumen y controlar el volumen circulante efectivo. Deplección de volumen. Si no existe contraindicación y de una manera simple, se puede realizar una rehidratación rápida (en unos 30 minutos) con 500-1000 ml de suero salino fisiológico, controlando la presión arterial, la presión venosa central si es posible y vigilando la respuesta clínica y diurética. Posteriormente se continuará la corrección del estado de hidratación dependiendo de la situación clínica de cada caso en particular. Disminución del volumen circulante efectivo. Se aplicaran los protocolos de tratamiento de los distintos tipos de shock, de la insuficiencia cardiaca, etc., correspondiente a cada situación clínica concreta y que han sido desarrollados en otra parte de este libro. (F., 2010)
- 8. IRA obstructiva El único tratamiento de urgencia es la desobstrucción e incluye fundamentalmente: El sondaje vesical por via urteral, o si es necesario suprapubica ,en los casos de patología prostatica. La nefrostomia percutánea en los casos de obstrucción supravesical. IRA parenquimatosa En los casos de IRA secundaria a patología glomerular, intersticial, vascular, etc., se aplicaran los protocolos específicos para cada caso, lo que escapa del objetivo de este libro. Tratamiento conservador de la IRA establecida Tratamiento de la Necrosis Tubular Aguda Como previamente hemos reiterado la IRA establecida y concretamente la necrosis tubular aguda que ocurre en las UCI, es consecuencia del efecto sumatorio de varios factores contribuyentes, tales como hipotensión, sepsis, fármacos nefrotóxicos y uso de la ventilación artificial con presión positiva intratorácica, entre otros. En esta situación, una serie de medidas pueden, sino evitar la necesidad de terapia renal sustitutoria mediante hemodiálisis, o diálisis peritoneal por ejemplo, si al menos transformar una IRA oligúrica en otra no oligúrica lo que permitirá cuanto menos un mejor manejo del enfermo. Estas medidas son generales e inespecíficas y se dirigen a crear un “ambiente favorable” que permita la pronta restitución de la función renal. Muchas de ellas fueron expuestas al hablar de la prevención de la IRA. Comentamos 3 aspectos fundamentales al estudiar la fisiopatología de la NTA: 1º.- Pérdida de la autorregulación de la perfusión renal, que puede agravarse por ejemplo con medicaciones vasoactivas mal empleadas (vasoconstrictoras de la arteria aferente glomerular como los AINEs o dilatadoras de la arteriola eferente como los IECAs), disminuciones de presión arterial secundarias a deplección de volumen, hemorragias o deficiente empleo de técnicas dialíticas, de forma que la hipoperfusión renal resultante, pude agravar o inducir daño tubular recurrente. 2º.- La mayor parte del consumo de oxígeno en el riñón es consecuencia de la reabsorción de sodio y de la concentración de la orina. Existe evidencia de que, reduciendo este trabajo, puede impedirse en parte la lesión tubular. Todas las situaciones de hipoperfusión son un estímulo muy importante para la reabsorción de sodio, por lo que evitarlas (incluyendo el uso innecesario de fármacos nefrotóxicos o contrastes radiológicos), es de nuevo una exigencia obligatoria en el manejo del paciente con IRA.
- 9. 3º.- En muchas formas de IRA existe una disociación entre la situación de la hemodinámica renal y la sistémica (sepsis, pancreatitis, insuficiencia hepática, disfunción multiorgánica) en el sentido de que existe vasoconstricción a nivel renal y una vasodilatación a nivel sistémico. El uso juicioso de catecolaminas vasocontrictoras, puede reducir el tono simpático reflejo y dar lugar a una vasodilatación paradójica de la vasculatura renal, con la consiguiente mejoría del funcionalismo de este órgano. (Gainza, 2015) Suplementos de bicarbonato de sodio para el tratamiento de la insuficiencia renal aguda En un estudio de 119 pacientes se comprobó la reducción del riesgo absoluto de 11,9% a 0,13 con la infusión de bicarbonato de sodio, lo que motivo que el estudio fuese interrumpido precozmente debido al grado de beneficio demostrado. Los beneficios del uso de bicarbonato de sodio por ejemplo son: Ayuda a aumentar los líquidos a través del cuerpo y por lo tanto ayuda a los riñones a procesar y eliminar el ácido úrico en exceso de tu sistema de forma más eficaz. Mejora la solubilidad de ácido úrico y por lo tanto acelera su recuperación. Eleva el pH de la sangre que sabemos ayuda a disminuir el riesgo de desarrollar cálculos renales. (Hewi, 2013) El mal uso de la dopamina en la insuficiencia renal aguda La Dopamina es una catecolamina sintética con actividad agonista directa e indirecta sobre los receptores alfa, beta y dopaminérgicos. Produce una activación diferencial perfectamente definida sobreestos subtipos de receptores, según su dosis, lo cual rige sus efectos funcionales que dependen de la dosis. Cuando se administra la dopamina a dosis bajas, vale decir a menos de 5 mcg/kg/minuto, activa los receptores dopaminérgicos existentes en la circulación renal, mesentérica y cerebral, con lo cual aumenta el flujo sanguíneo en estas regiones. La literatura en Adultos: 1) Kellum y Decker realizan una meta-análisis sobre el uso de la dopamina en dosis bajas en pacientes con insuficiencia renal aguda
- 10. (IRA)) para evaluar el impacto de este fármaco en la prevención, desarrollo y curso de la IRA, la mortalidad y los requerimientos de hemodiálisis en pacientes en estado crítico. De los 58 estudios evaluados por estos autores, los mismos publicados durante los últimos 33 años, en 24 de ellos se comunicaron uno o más datos de evolución primaria; en el análisis fueron incluidos 17 ensayos randomizados y controlados (854 pacientes). No existieron diferencias en cuanto a mortalidad entre los receptores de dopamina y los que recibieron placebo (11 ensayos, n=508). Tampoco las hubo en relación con el desarrollo de IRA (11 ensayos, n=511), ni con la necesidad de hemodiálisis (10 ensayos, n=618), concluyendo que la dopamina en dosis bajas en pacientes con enfermedad crítica e insuficiencia renal aguda, o con riesgo de sufrirla, no reduce la incidencia ni limita la mortalidad, o la necesidad de hemodiálisis; y por lo tanto, la Dopamina debe ser eliminada de la rutina clínica para esta indicación. (Carrasco, 2010) Bibliografía Carrasco, D. O. (03 de Agostode 2010). EL MALUSODE LA DOPAMINA EN LA INSUFICIENCIA RENAL AGUDA. Obtenidode Hospitalde Clinicas: http://www.ops.org.bo/textocompleto/facmed/chc2004490111.pdf F.,B. R. (14 de Agostode 2010). Acetilcisteína para prevenirfalla renal pormedio decontraste. Obtenidode Eclipse: http://escuela.med.puc.cl/recursos/mbe2001/eclipseAcetilcisteina.html Gainza,F. (10 de Septiembrede 2015). Insuficiencia renalaguda. Obtenidode Hospitalde Cruces:http://nefrologiadigital.revistanefrologia.com/es-monografias-nefrologia-dia- articulo-insuficiencia-renal-aguda-25 Hewi,J.(06 de Juliode 2013). Sodiumbicarbonatesupplementsfortreating acutekidney injury. Obtenidode Cochrane: http://onlinelibrary.wiley.com/doi/10.1002/14651858.CD009204/abstract;jsessionid= AAEA2CA2E5531AECD766CCFE9C998FC5.f01t01 Mehran,R. (12 de Octubre de 2012). N-acetilcisteína en la prevención de la nefropatía inducida porcontraste. Obtenidode Universidadde Columbia: http://www.revespcardiol.org/es/n-acetilcisteina-prevencion-nefropatia-inducida- por/articulo/13146212/ Needham,D.E.(06 de Mayo de 2012). Intramed. Obtenidode Insuficienciarenal aguda: http://www.intramed.net/contenidover.asp?contenidoID=40351&pagina=2 Ponce,M. A. (23 de Diciembre de 2014). medigraphic. Obtenidode Insuficienciarenal aguda (IRA) yterapiade reemplazorenal temprano(TRR): http://www.medigraphic.com/pdfs/medcri/ti-2013/ti134h.pdf
