8.0 8.1 sistemas biologicos de oxido reduccion
•Descargar como ODP, PDF•
3 recomendaciones•5,104 vistas
Una reacción de óxido-reducción implica la transferencia de electrones entre sustancias, donde una sustancia gana electrones (reducción) y otra pierde electrones (oxidación). La oxidación aumenta el estado de oxidación al perder electrones, mientras que la reducción disminuye el estado de oxidación al ganar electrones. Dentro de una reacción redox, existen semirreacciones parciales de reducción y oxidación.
Denunciar
Compartir
Denunciar
Compartir
Recomendados
Más contenido relacionado
La actualidad más candente
La actualidad más candente (20)
Balanceo de Ecuaciones Químicas: Metodo Redox tema 4

Balanceo de Ecuaciones Químicas: Metodo Redox tema 4
Informe practica #3 (articulo cientifico), Clasificacion de sustancias organi...

Informe practica #3 (articulo cientifico), Clasificacion de sustancias organi...
Tema 13 - Reactividad de los compuestos del carbono

Tema 13 - Reactividad de los compuestos del carbono
Similar a 8.0 8.1 sistemas biologicos de oxido reduccion
Similar a 8.0 8.1 sistemas biologicos de oxido reduccion (20)
Ganar o perder electrones no es problema para ninguna sustancia

Ganar o perder electrones no es problema para ninguna sustancia
Importanciadelasreaccionesredox 140308220046-phpapp01

Importanciadelasreaccionesredox 140308220046-phpapp01
Bioquimica II, procesos redox en los seres vivos leyes termodinamica

Bioquimica II, procesos redox en los seres vivos leyes termodinamica
Bioquimica II, procesos redox en los seres vivos / leyes termodinamica

Bioquimica II, procesos redox en los seres vivos / leyes termodinamica
Más de Raul hermosillo
Más de Raul hermosillo (20)
Último
El 7 de junio de 1890, por ejemplo, Henry Marmaduke Harris obtuvo una patente británica (Nº 8816) para "Máquinas aéreas con aerostatos" en las que el "coche... en forma de barco" estaba unido a un globo y era "impulsado por la reacción de los gases descargados a través de una boquilla... cuya dirección estaba controlada, relacionada con algún tipo de dispositivo o tecnología de dirección. ".1890 –7 de junio - Henry Marmaduke Harris obtuvo una patente británica (Nº 88...

1890 –7 de junio - Henry Marmaduke Harris obtuvo una patente británica (Nº 88...Champs Elysee Roldan
Último (20)
El Gran Atractor, la misteriosa fuerza que está halando a la Vía Láctea.pptx

El Gran Atractor, la misteriosa fuerza que está halando a la Vía Láctea.pptx
IAAS- EPIDEMIOLOGIA. antisepcsia, desinfección, epp

IAAS- EPIDEMIOLOGIA. antisepcsia, desinfección, epp
Soporte vital basico maniobras de soporte vital basico

Soporte vital basico maniobras de soporte vital basico
Glaeser, E. - El triunfo de las ciudades [2011].pdf![Glaeser, E. - El triunfo de las ciudades [2011].pdf](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
![Glaeser, E. - El triunfo de las ciudades [2011].pdf](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
Glaeser, E. - El triunfo de las ciudades [2011].pdf
1890 –7 de junio - Henry Marmaduke Harris obtuvo una patente británica (Nº 88...

1890 –7 de junio - Henry Marmaduke Harris obtuvo una patente británica (Nº 88...
Trichomonas es un género de parásitos protozoarios flagelados.

Trichomonas es un género de parásitos protozoarios flagelados.
Mapa-conceptual-de-la-Seguridad-y-Salud-en-el-Trabajo-3.pptx

Mapa-conceptual-de-la-Seguridad-y-Salud-en-el-Trabajo-3.pptx
Hobson, John A. - Estudio del imperialismo [ocr] [1902] [1981].pdf![Hobson, John A. - Estudio del imperialismo [ocr] [1902] [1981].pdf](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
![Hobson, John A. - Estudio del imperialismo [ocr] [1902] [1981].pdf](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
Hobson, John A. - Estudio del imperialismo [ocr] [1902] [1981].pdf
El Genoma Humano, Características, Definición, ETC

El Genoma Humano, Características, Definición, ETC
Antequera, L. - Historia desconocida del descubrimiento de América [2021].pdf![Antequera, L. - Historia desconocida del descubrimiento de América [2021].pdf](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
![Antequera, L. - Historia desconocida del descubrimiento de América [2021].pdf](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
Antequera, L. - Historia desconocida del descubrimiento de América [2021].pdf
8.0 8.1 sistemas biologicos de oxido reduccion
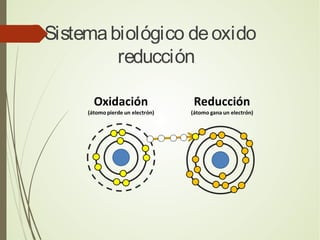
- 2. Oxido ReducciónOxido Reducción Una reacción de óxido-reducción se caracteriza porque hay una transferencia de electrones, en donde una sustancia gana electrones y otra sustancia pierde electrones: • la sustancia que gana electrones disminuye su número de oxidación. Este proceso se llama Reducción. • la sustancia que pierde electrones aumenta su número de oxidación.Este proceso se llama Oxidación. Por lo tanto, la Reducción es ganancia de electrones y la Oxidación es una pérdida de electrones.
- 3. • En el proceso de oxido reducción se conoce los siguiente participantes Agente oxidante :retira electrones de una molécula que puede donarlos .al final de este compuesto se reduce Agente reductor: dona electrones a otras moléculas . Al fina de este proceso este compuesto se oxida
- 4. Principio de electro neutralidad El principio de electro neutralidad de Pauling corresponde a un método de aproximación para estimar la carga en moléculas o iones complejos, este supone que la carga siempre se distribuye en valores cercanos a 0 (es decir, -1, 0, +1). Dentro de una reacción global redox, se da una serie de reacciones particulares llamadas semirreacciones o reacciones parciales. •Semirreacción de reducción: 2e− + Cu2+ → Cu0 •Semirreacción de oxidación: Fe0 → Fe2+ + 2e− La tendencia a reducir u oxidar a otros elementos químicos se cuantifica por el potencial de reducción, también llamado potencial redox. Una titulación redox es una en la que un indicador químico indica el cambio en el porcentaje de la reacción redox mediante el viraje de color entre el oxidante y el reductor.
Notas del editor
- <número>
- <número>