Taller de nivelacion i periodo once
- 1. Fecha: Docente: Anderson Osorio Sierra Periodo: Primero Grado: Once Asignatura: Química Área: Ciencias Naturales TALLER DE NIVELACIÓN PARA EL I PERIODO ACADÉMICO – GRADO ONCE 1. 2.
- 2. 3. Una persona ha bebido 153,5 ml de una bebida alcohólica, cuya graduación alcohólica es 40 N (40 gr de alcohol/100ml) de licor. Sabiendo que el 15% de alcohol ingerido pasa al torrente sanguíneo, que el volumen de sangre de este adulto es de 5 litros de sangre y que la concentración considerada toxica es de 0,0036 gr alcohol/ml sangre. Indicar si esta persona esta intoxicada o no. 4. Se mezclan 3,54 lt de alcohol en 25 lt de agua ¿Cuál es el %v/v de agua y de alcohol? 5. Cuantos gramos de agua se requieren para disolver 0,072 moles de K2CO3 y obtener una solución al 3 % p/p? 6.
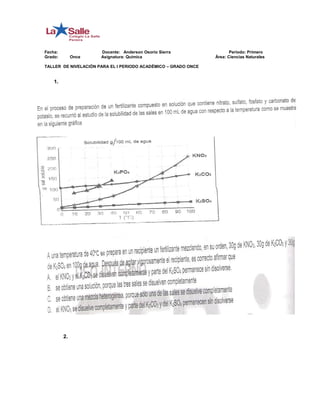
- 3. 7. El suero fisiológico es una solución acuosa de cloruro de sodio (NaCl) de concentración 7,95 gr NaCl/dm3 . Calcular la masa de NaCl que ingresa en el organismo de un paciente al que se le administra suero durante 3,5 horas con una velocidad de goteo de 1 gota por segundo (1 gota/seg). Nota: considerar el volumen de una gota: 0,06 cm3 . 8. Un desinfectante de uso doméstico. Tiene una concentración de 10 % v/v de Hipoclorito de sodio. 45 % v/v de vinagre. Y el resto es alcohol. ¿Cuántos cm3 habrá que tomar de cada sustancia para obtener 400 cm3 de solución desinfectante? 9. Cuantos gramos de agua se requieren para disolver 0,08 moles de NaCl y obtener una solución al 4,5 % p/p? 10. En la grafica se muestra la dependencia de la solubilidad de dos compuestos ionicos en agua, en funcion de la temperatura.
- 4. Se preparo una mezcla de sales, utilizando 90 gramos de KNO3 y 10 gramos de NaCl. Esta mezcla se disolvio en 100 gr de H2O y se calento hasta 60 o C, luego se dejo enfriar gradualmente hasta 0 0 C. es probable que al final del proceso. a. Se obtenga un precipitado de NaCl y KNO3 b. Se obtenga un precipitado de NaCl. c. Se obtenga un precipitado de KNO3. d. Los componentes de la mezcla permanezcan disueltos. 11. Cuantos gramos de solvente (H2O), se requieren para preparar una solución de 20% de CuSO4 por masa (%p/p) que contenga 80 gramos de soluto. Responda las preguntas 12 y 13 con la siguiente información. La solubilidad es la máxima cantidad de soluto que se disuelve en 100 gramos de un solvente, a una temperatura dada. En la gráfica se ilustra la solubilidad de un soluto X en un solvente Y en función de la temperatura. 12. Un estudiante desea preparar una solución saturada de X en Y, para ello debe disolver, mínimo. A. 30 gramos de X en 100 g. de Y a 50°C B. 15 gramos de X en 100 g. de Y a 30 °C C. 5 gramos de X en 100 g. de Y a 0°C D. 20 gramos de X en 100 g. de Y a 50 °C 13. Es válido afirmar que al mezclar 20 g de X con 100 g de Y se forma una. A. Solución a 20 °C B. Mezcla heterogénea a 50 °C
- 5. C. Solución a 30 °C D. Mezcla heterogénea a 35 ° C 14. Calcule la Molaridad de H3PO4 , cuya densidad es 1,75 g/ml, y concentración por peso es de 93% p/p, en 2 L de solución. 15. Cuantos gramos de soluto hay en 850 ml de H2SO4 2,5 N. 16. Cuantos ml de solución se requieren para preparar una concentración de 3,2ppm, sabiendo que tiene 0,23 gramos de Na+. 17. Si se agregan 75 g de sustancia Y, en 100 g de agua, a 80°C, de acuerdo con la gráfica se puede decir que. A. 15 g de sustancia Y permanece sin disolver. B. la sustancia Y se disuelve totalmente. C. la sustancia Y permanece sin disolver. D. a sustancia Y inicialmente se disuelve y después precipita en su totalidad 18. A 60 °C, la solubilidad del Cloruro de Potasio (KCl) es de 45,5 gramos en 100 gramos de agua; y a 10 °C, la solubilidad es de 31,0 gramos en 100 gramos de agua. A 60 °C, se tiene una solución saturada de 45,5 gramos de KCl en 100 gramos de agua. Al disminuir la temperatura hasta 10 °C, se espera que.
- 6. A. permanezca disuelto todo el KCl. B. 31,0 gramos de KCl no se solubilicen. C. 14,5 gramos de KCl no se solubilicen. D. solo la mitad de KCl se solubilice.
- 7. A. permanezca disuelto todo el KCl. B. 31,0 gramos de KCl no se solubilicen. C. 14,5 gramos de KCl no se solubilicen. D. solo la mitad de KCl se solubilice.
