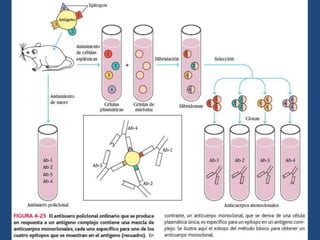
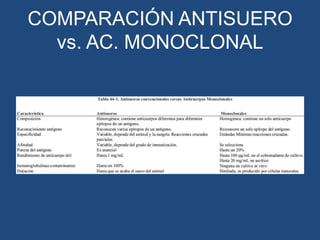
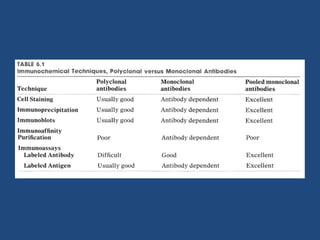
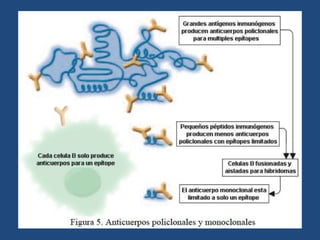
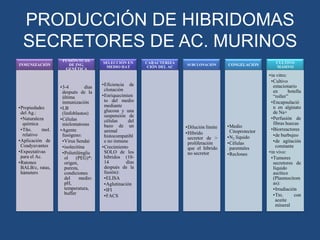
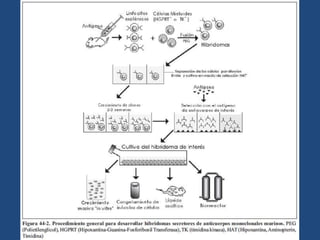
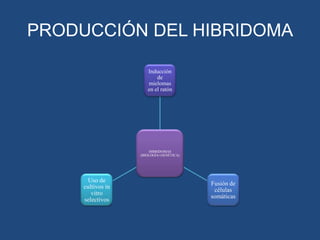
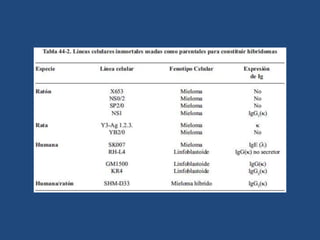
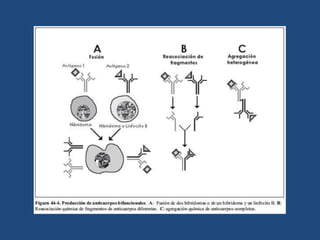
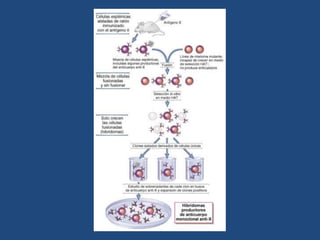
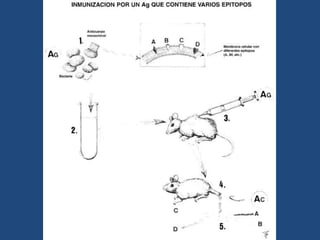
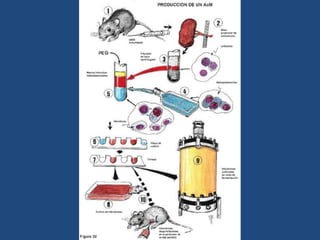
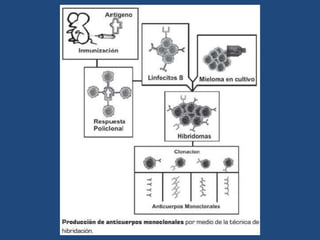
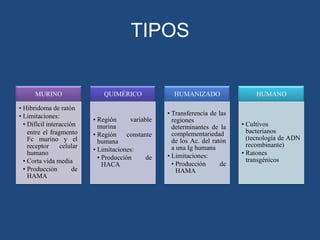
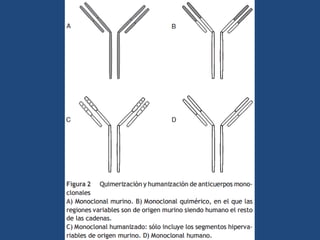
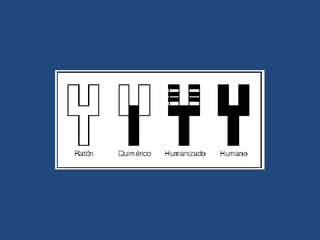
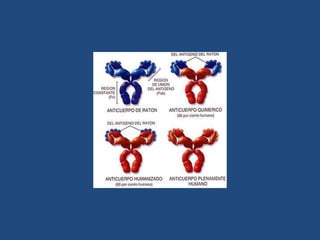
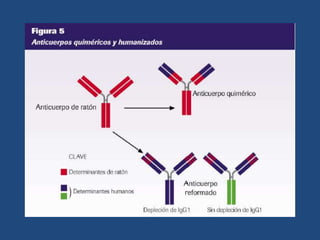
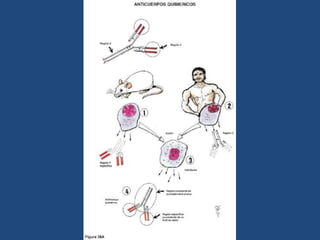
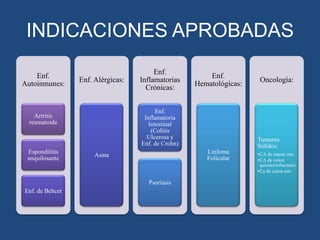
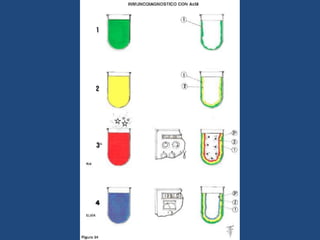
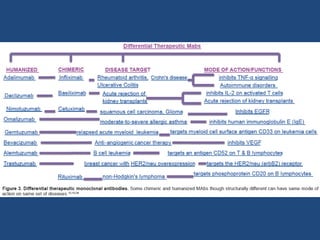
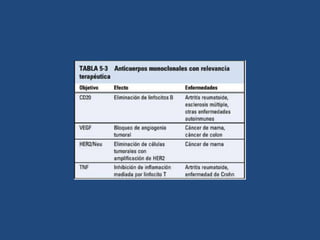
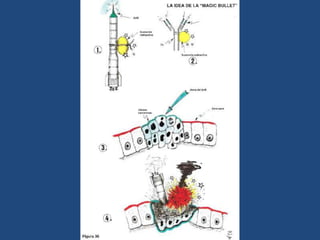
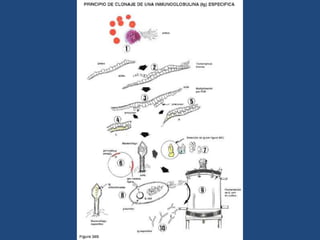
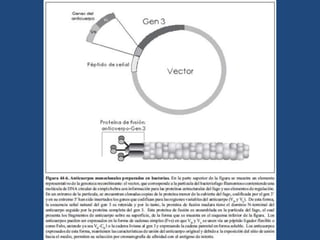
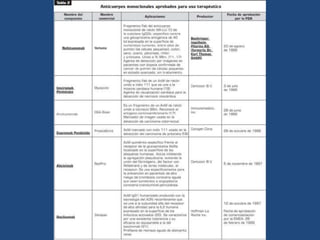
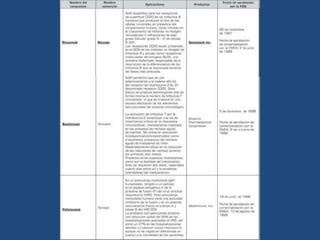
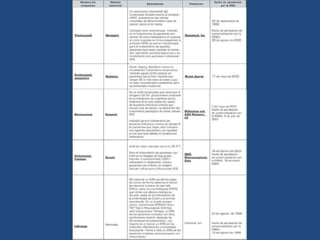
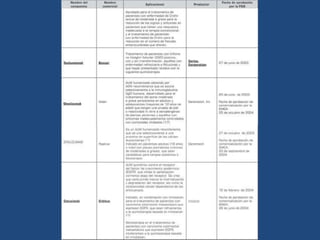
Este documento proporciona una introducción general a los anticuerpos monoclonales (mAb). Explica que los mAb son anticuerpos específicos para un solo epítopo producidos mediante la fusión de linfocitos B con células mielomatosas. Detalla el proceso de producción de hibridomas y la importancia clínica de los mAb en aplicaciones como el diagnóstico, la terapéutica y la investigación médica.