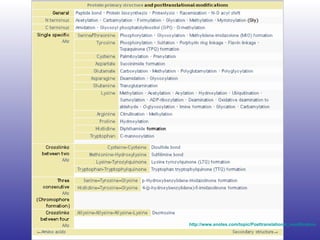
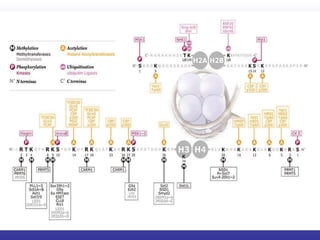
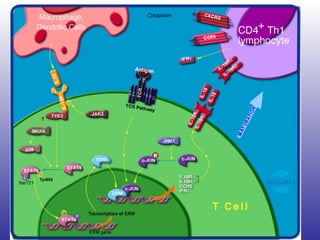
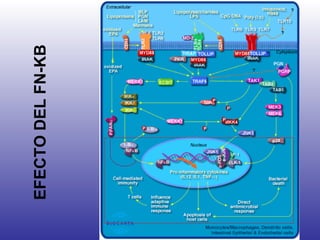
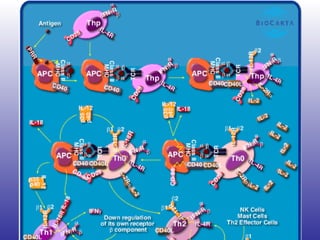
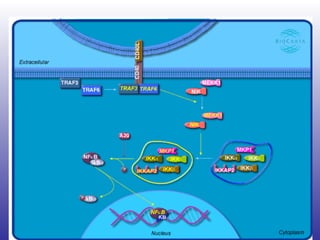
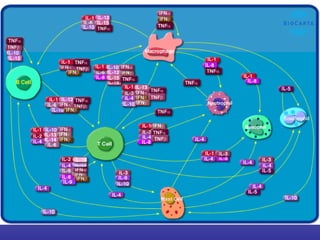
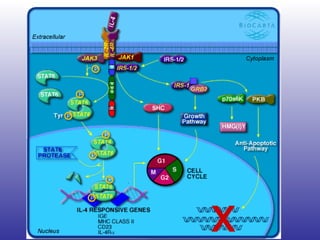
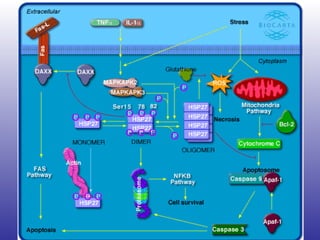
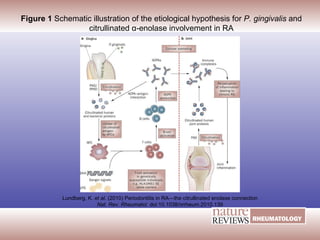
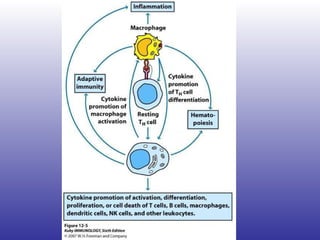
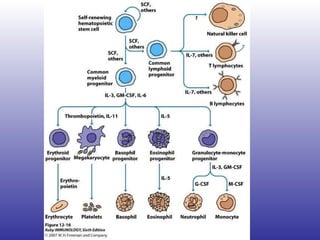
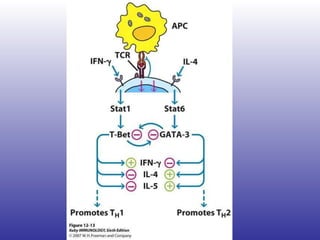
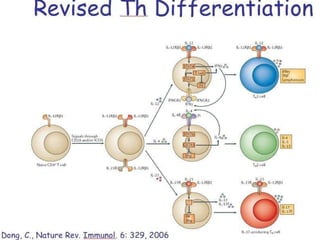
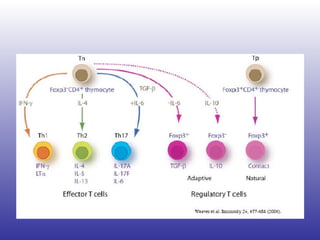
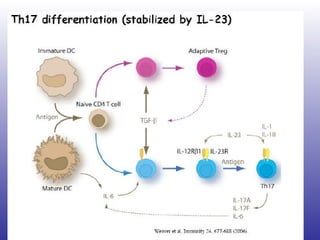
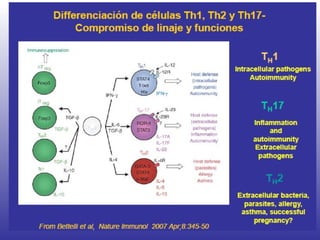
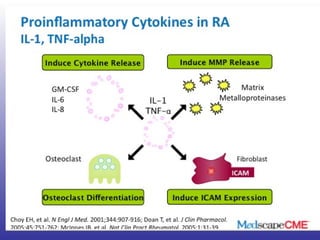
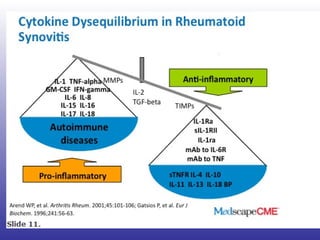
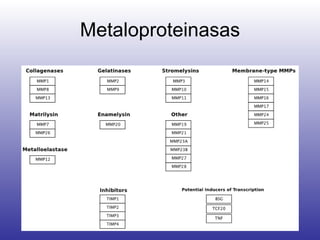
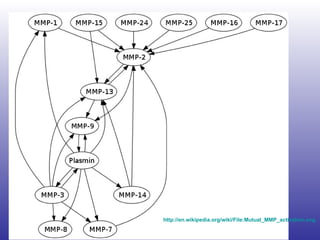
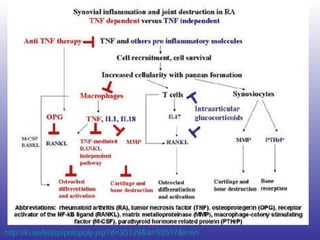
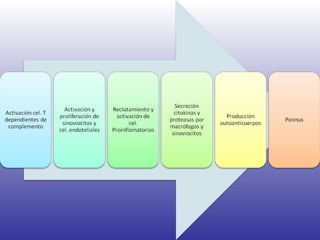
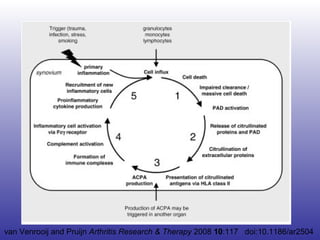
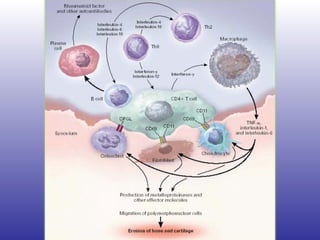
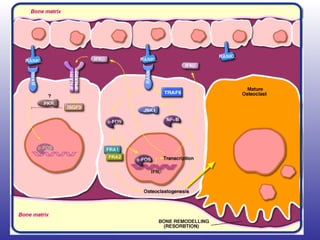
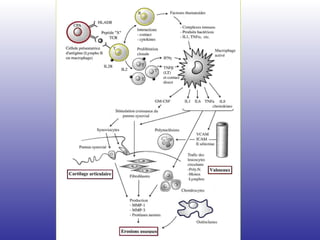
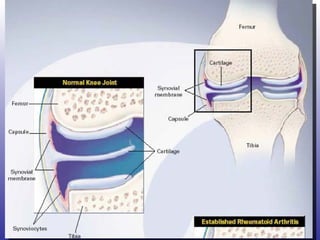
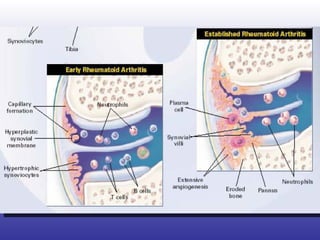
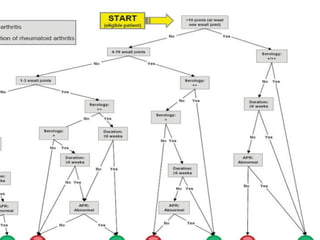
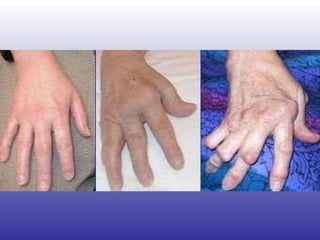
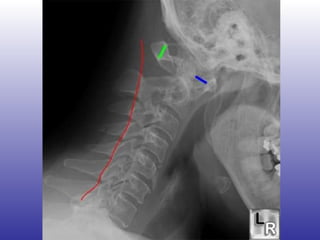
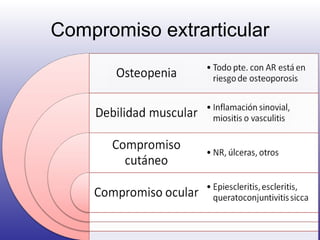
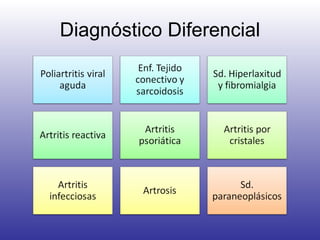
El documento aborda la artritis reumatoide (AR), incluyendo su historia, epidemiología, factores de riesgo como la susceptibilidad genética y el tabaquismo, y su etiología. Se discuten los mecanismos inmunológicos involucrados, como la activación de linfocitos T y la producción de autoanticuerpos, además de la importancia del diagnóstico temprano para prevenir daños articulares irreversibles. También se examinan opciones de tratamiento y el pronóstico a largo plazo de los pacientes con AR.













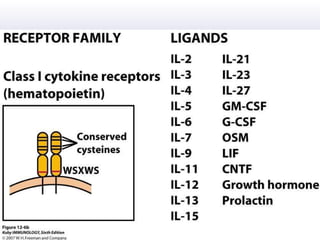

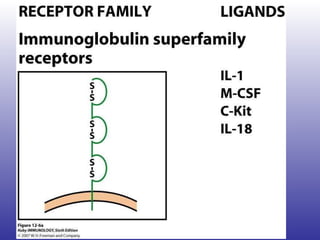
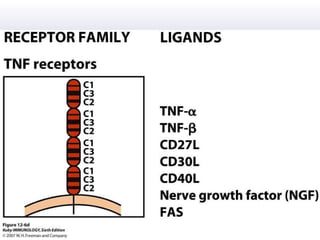
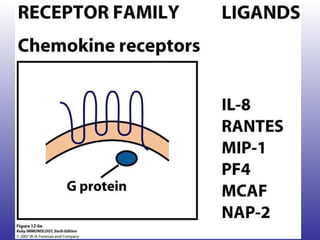



















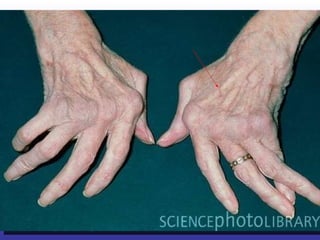

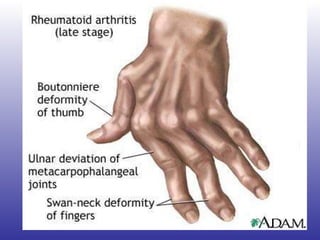
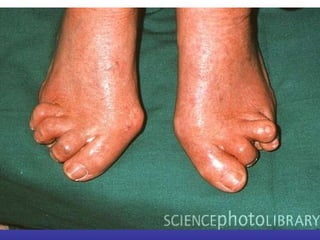
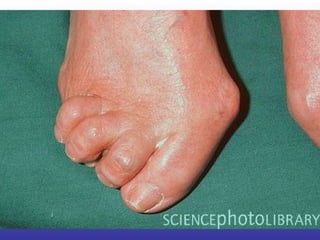
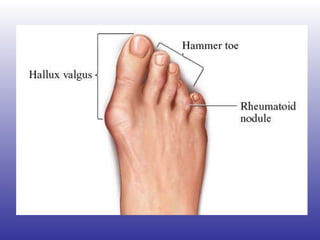
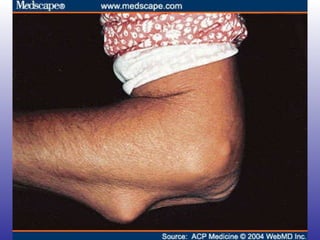
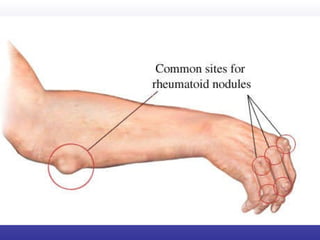






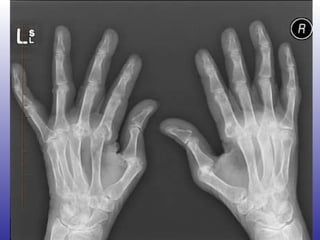






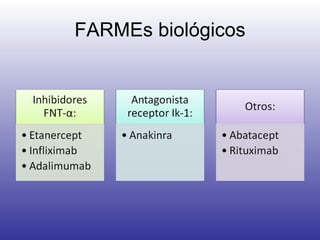




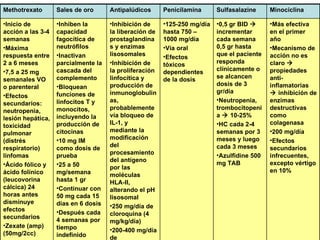
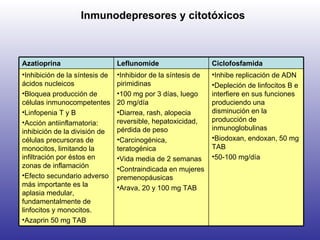
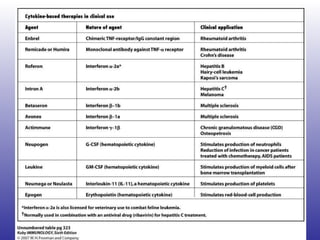



![“ The list of medications considered safe during pregnancy, according to the most recent evidence, includes steroids, hydroxychloroquine, sulphasalazine, and azathioprine. Unsafe drugs are methotrexate, leflunomide, and biologics (anti–tumor necrosis factor [TNF] agents and rituximab).”](https://image.slidesharecdn.com/artritisreumatoidea2011-hesv-110928174224-phpapp02/85/Artritis-reumatoidea-2011-hesv-125-320.jpg)