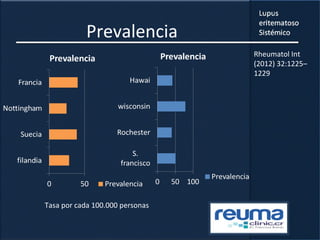
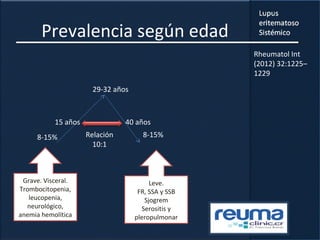
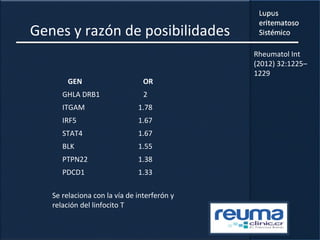
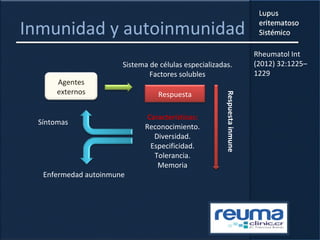
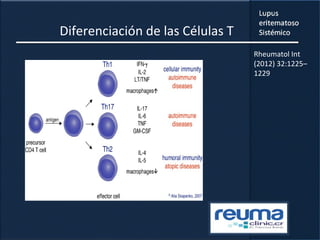
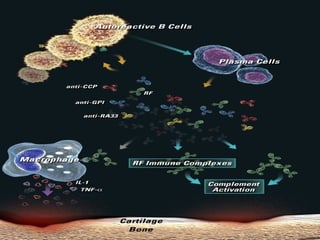
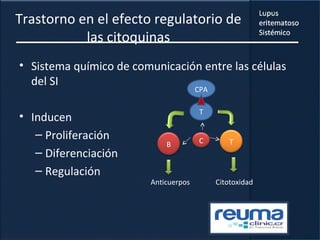
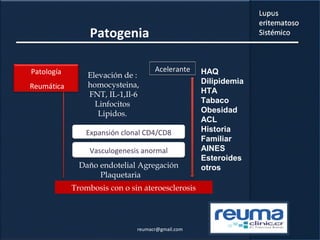
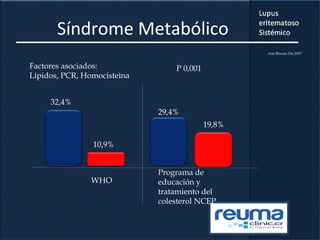
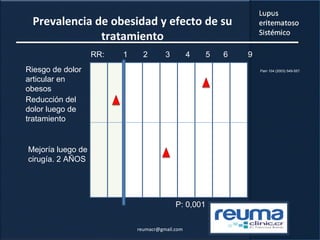
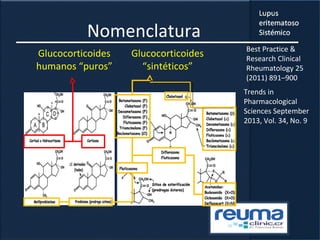
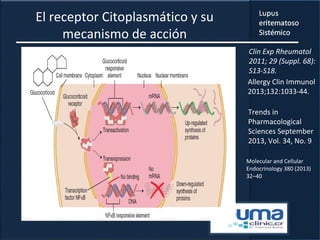
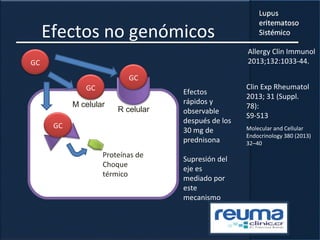
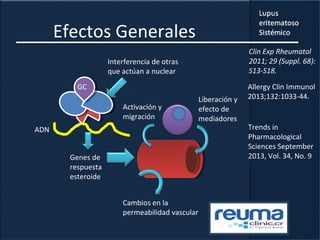
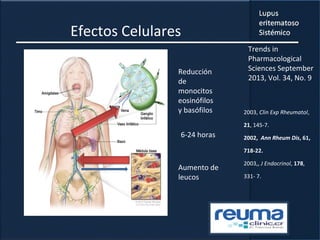
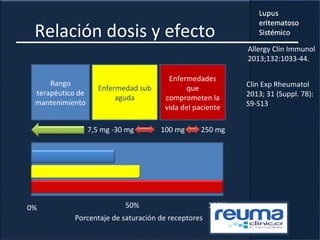
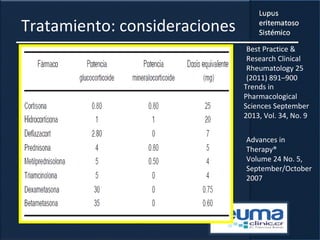
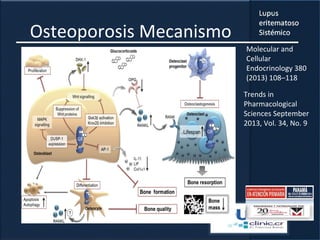
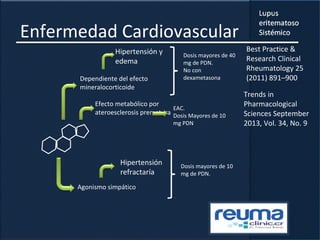
1) El documento presenta información sobre el lupus eritematoso sistémico, incluyendo su incidencia, prevalencia, factores genéticos, efectos hormonales, patogenia, síntomas, manifestaciones, criterios de diagnóstico y comorbilidades.
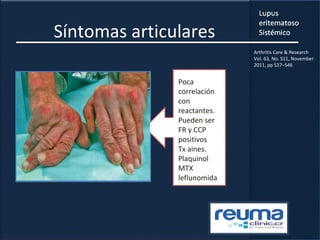
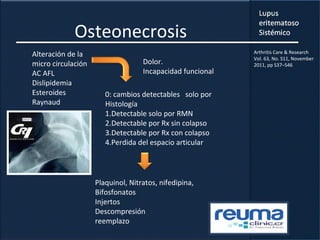
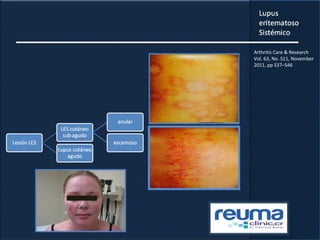
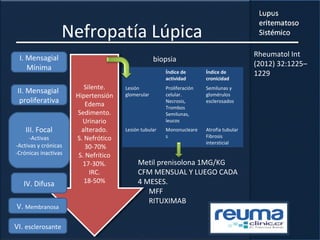
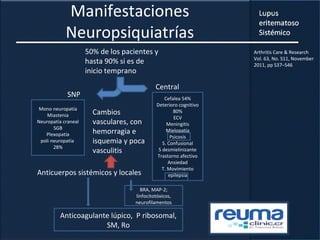
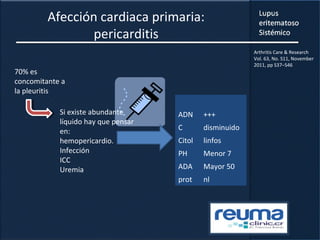
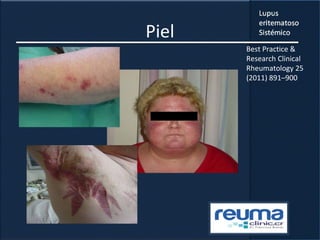
2) Se describen varios síntomas como fatiga, artritis, osteonecrosis, manifestaciones renales y hematológicas.
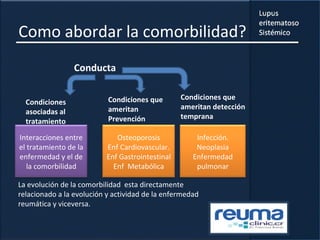
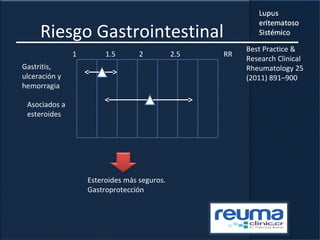
3) La comorbilidad tiene un impacto importante en la mortalidad, hospitalizaciones, incapacidad y costos de los pacientes con lupus