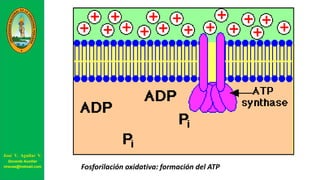
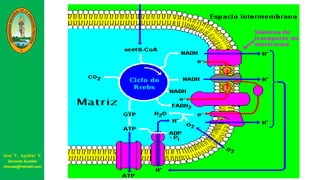
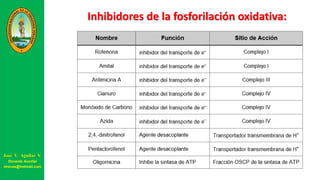
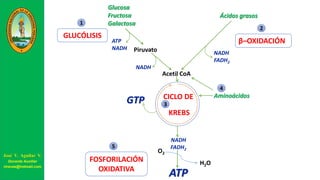
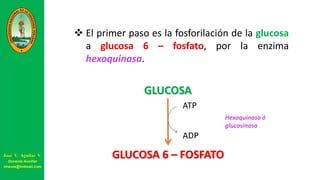
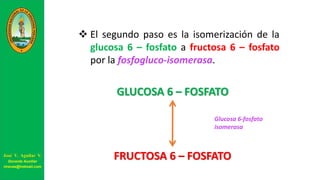
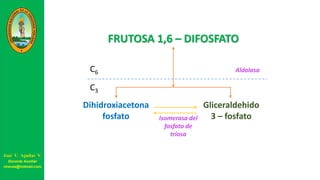
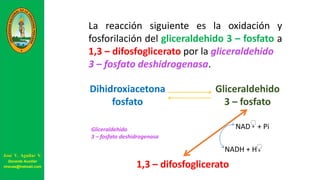
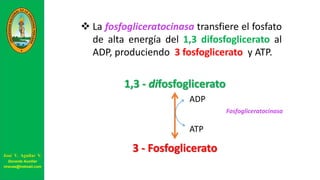
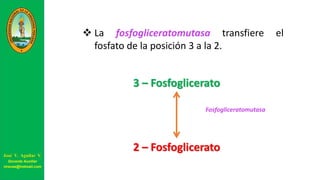
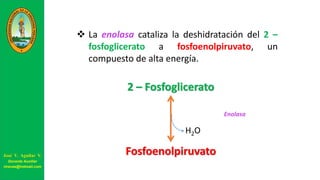
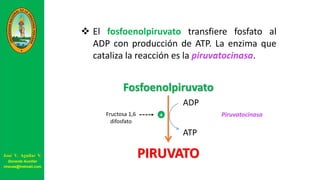
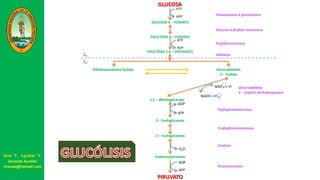
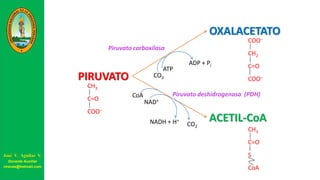
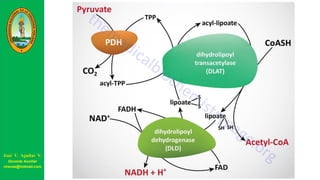
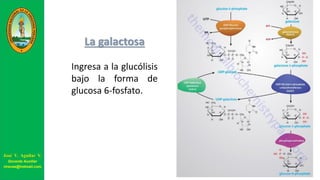
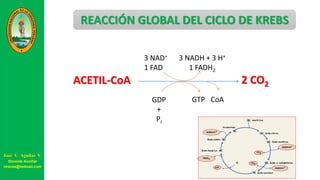
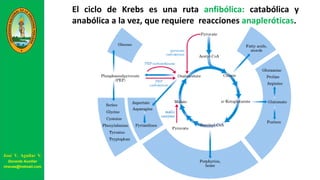
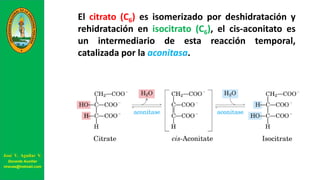
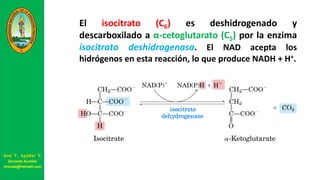
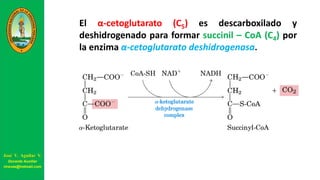
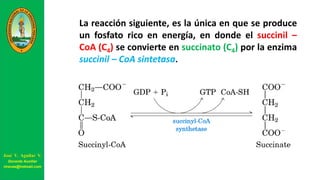
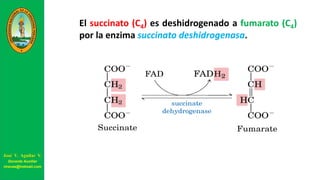
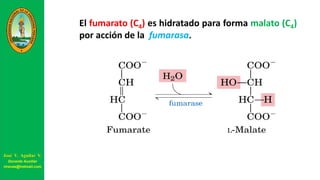
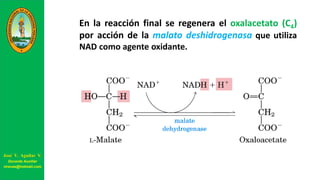
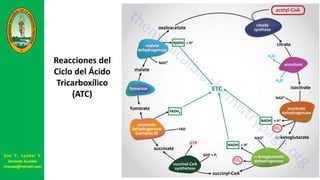
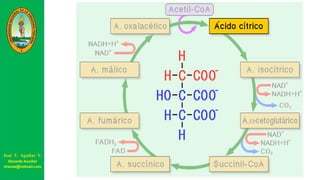
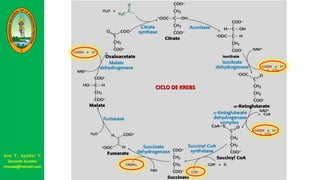
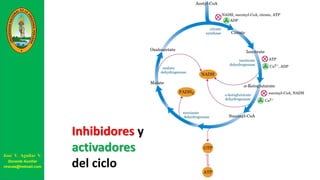
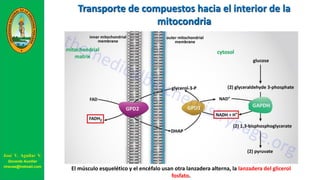
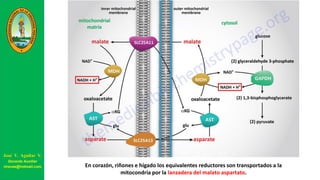
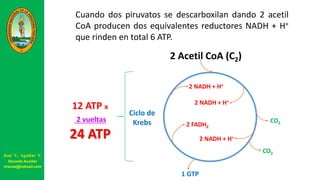
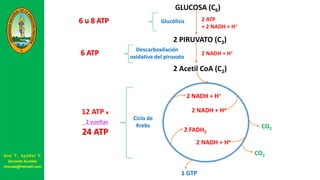
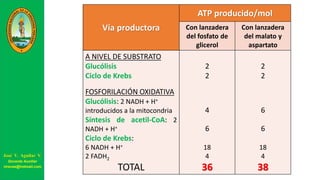
Este documento describe las principales vías metabólicas de producción de ATP y NADH, incluyendo la glucólisis, oxidación de ácidos grasos, ciclo del ácido cítrico y cadena de transporte de electrones. Explica detalladamente cada una de las etapas de la glucólisis y del ciclo del ácido cítrico, así como los coenzimas involucrados. También menciona que estas vías sirven para degradar carbohidratos, lípidos y aminoácidos con fines energéticos y sintéticos.


















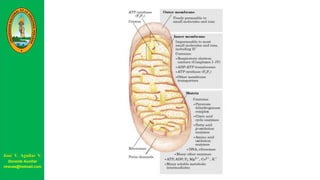




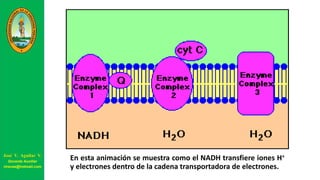
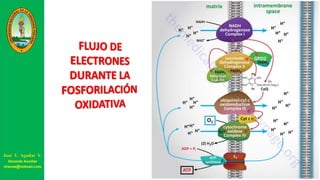



![Gradiente de protones: las cargas + son retiradas
del interior mientras que las – permanecen en el
interior (en gran parte como iones OH- ).
[El pH en la cara externa de la membrana puede
llegar a un pH 5.5, mientras que el pH justo en la
cara interna de la misma puede llegar a 8,5. ]
José V. Aguilar V.
Docente Auxiliar
viravas@hotmail.com](https://image.slidesharecdn.com/cap-140712140218-phpapp01/85/Cap-4-catabolismo-oxidativo-61-320.jpg)