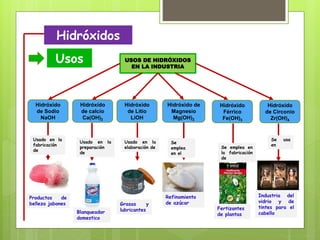
Este documento describe los hidróxidos inorgánicos, compuestos formados por un catión metálico unido al ión hidróxido. Explica que los hidróxidos neutralizan los ácidos, son solubles en agua y se usan en industrias como la fabricación de jabones, vidrio y fertilizantes. Además, detalla diferentes métodos de nomenclatura de los hidróxidos, incluyendo la forma tradicional y sistemática.