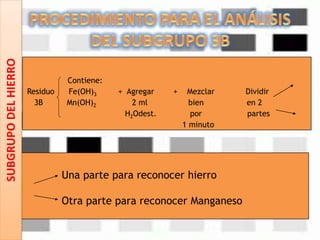
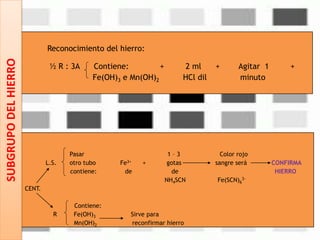
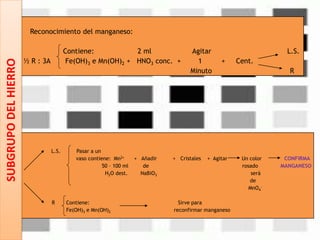
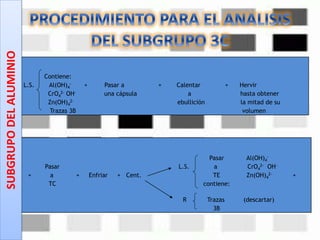
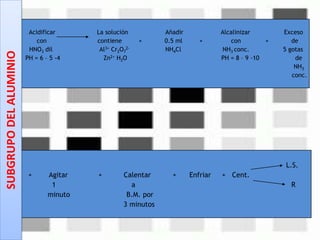
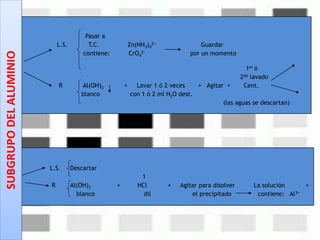
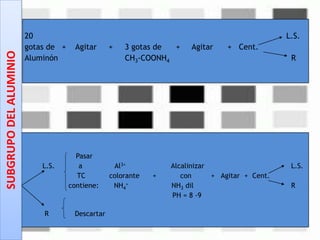
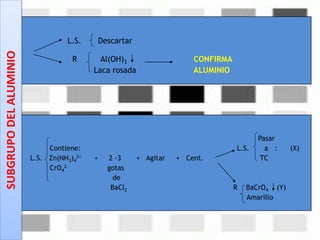
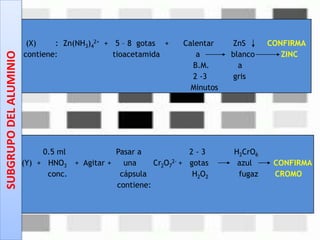
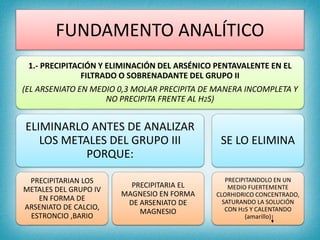
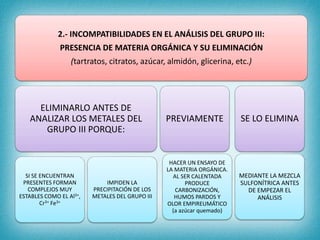
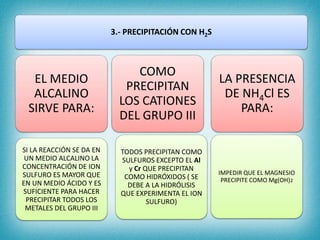
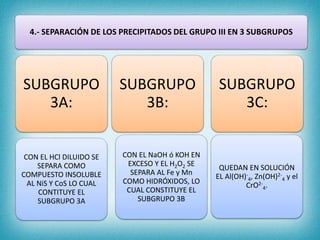
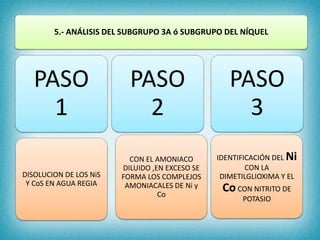
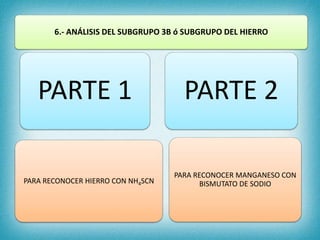
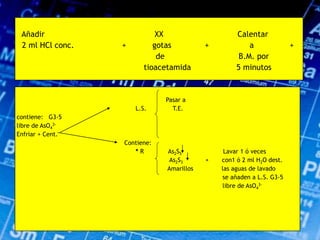
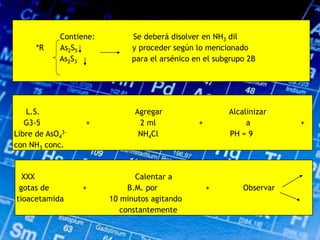
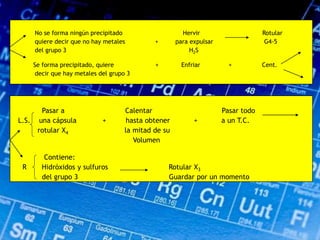
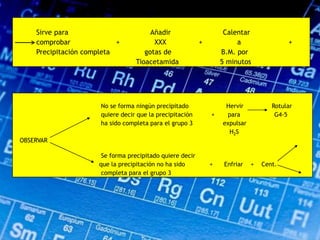
Este documento describe los pasos para realizar el análisis cualitativo de cationes del Grupo III, incluyendo la precipitación con H2S, la separación en tres subgrupos, y el análisis de cada subgrupo para identificar níquel, hierro, manganeso, aluminio y cromo. Explica cómo eliminar interferencias de arsénico y materia orgánica antes del análisis, y los reactivos y pruebas utilizados para identificar cada ión metálico.



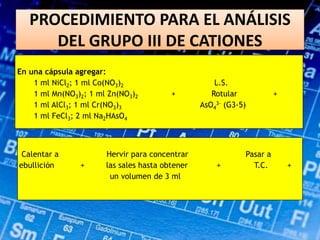




![Agitar para 1 ml Calentar
disolver la sal + KNO2 + a + Enfriar + Cent.
6M B.M por
1 minuto
L.S. Descartar
R K3[Co(NO2)6] CONFIRMA COBALTO
Amarillo
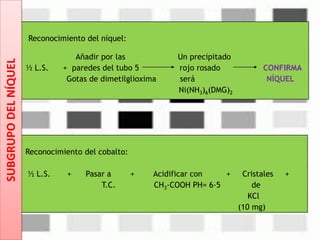
SUBGRUPODELNÍQUEL](https://image.slidesharecdn.com/clase10-marchag-32clases-150511042236-lva1-app6892/85/Clase-10-marcha-g-3-2-clases-24-320.jpg)