El documento proporciona instrucciones para realizar pruebas químicas cualitativas de cationes de los grupos III, incluyendo Mn2+, Ni2+, Co2+ y Zn2+. Describe las reacciones, cambios de color y precipitados observados al agregar reactivos como amoníaco, hidróxido de sodio, sulfuro de hidrógeno, bismutato de sodio y otros a muestras de los cloruros y nitratos de estos cationes. El objetivo es identificar los cationes mediante la comparación de los resultados observados con




![TÉCNICA
1) V gotas de solución
muestra
2) ½ mL de agua
destilada
3) ½ mL de NaOH-
KOH 2M
5) Probar solubilidad
con HCl 3M (también
soluble en NH3)
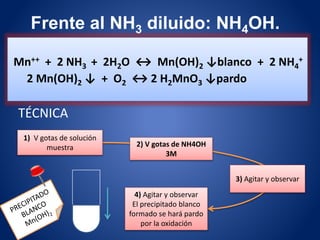
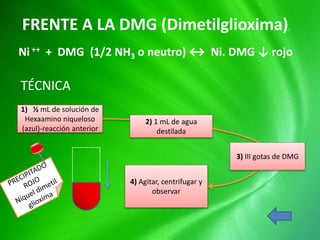
Frente al NaOH-KOH 2M.
Ni++ + 2OH- ↔ Ni(OH)2 ↓verde claro/gelatinoso
Ni(OH)2 ↓ + 2 H+ ↔ Ni++ + 2 H2O
Ni(OH)2 ↓ + 6 NH3 ↔ [ Ni (NH3)6 ]++/azul + 2 OH–
4) Centrifugar –
descartar
sobrenadante](https://image.slidesharecdn.com/clase9-cationesg3-2parte-zn-mn-co-ni-150511041726-lva1-app6891/85/Clase-9-cationes-g3-2-parte-zn-mn-co-ni-12-320.jpg)
![TÉCNICA
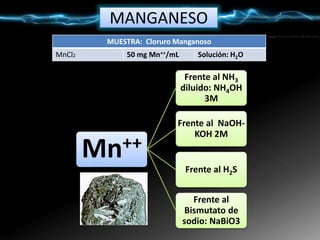
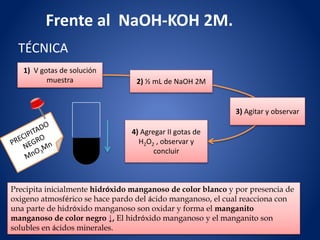
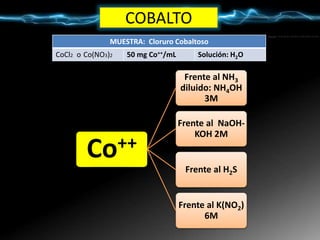
Frente al NH3 diluido: NH4OH.
Ni++ + NH3 + H2O + Cl- ↔ Cl OH Ni ↓verde
ClOHNi ↓ + exceso 6 NH3 ↔ [ Ni (NH3)6 ] ++/azul + Cl - + OH–
1) V gotas de solución
muestra 2) III gotas de NH4OH
3M
3) Una vez que precipite
(verde) agregar exceso de
reactivo hasta disolución4) De precipitado
verde pasara a una
solución de coloración
azul
GUARDAR PARA LA
PRUEBA CON DMG](https://image.slidesharecdn.com/clase9-cationesg3-2parte-zn-mn-co-ni-150511041726-lva1-app6891/85/Clase-9-cationes-g3-2-parte-zn-mn-co-ni-14-320.jpg)

![TÉCNICA
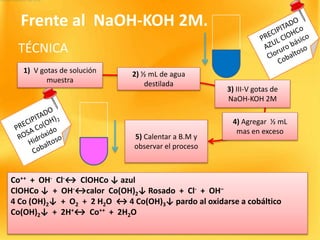
Frente al NH3 diluido: NH4OH.
Co++ + NH3 + H2O + Cl - ↔ ClOHCo ↓ azul + NH4
+
ClOHCo ↓ + exceso 6NH3 ↔ [Co (NH3)6]++ pardo + Cl - + OH–
[Co (NH3)6]++ (oso) /pardo O2 ↔ [Co(NH3)6]+++(ico)/ rojizo
1) V gotas de solución
muestra
2) V-X gotas de NH4OH
3M
3) Observar y concluir
INICIALMENTE
CON EXCESO
DE REACTIVO](https://image.slidesharecdn.com/clase9-cationesg3-2parte-zn-mn-co-ni-150511041726-lva1-app6891/85/Clase-9-cationes-g3-2-parte-zn-mn-co-ni-19-320.jpg)
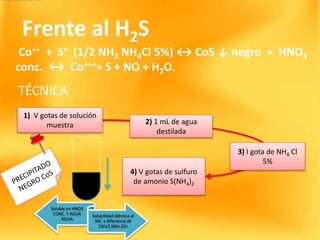
![FRENTE AL NITRITO DE POTASIO 6M.
Co++ + 7NO2
- + 3K+ + ½ 2 CH3COOH ↔ [Co (NO2)6] K3
↓amarillo + 2CH3COO- + NO + H2O
1) V gotas de solución
muestra 2) 1 mL de agua
destilada
3) I gota de Ácido
Acético
4) V-X gotas de KNO2
6M agitar, centrifugar y
observar
TÉCNICA](https://image.slidesharecdn.com/clase9-cationesg3-2parte-zn-mn-co-ni-150511041726-lva1-app6891/85/Clase-9-cationes-g3-2-parte-zn-mn-co-ni-21-320.jpg)

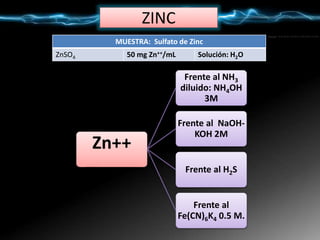
![Zn+2 + 2 OH- ↔ Zn(OH)2 ↓blanco/gelatinoso (anfótero)
Zn(OH)2 ↓ + exceso 2 OH- ↔ [Zn(OH)4]= ion cincato/incoloro
Zn(OH)2 ↓ + 2 H+ ↔ Zn++ + 2 H2O
Zn(OH)2 ↓ + 4 NH3 ↔ [Zn(NH3)]4]++ incoloro + 2 OH–
TÉCNICA
1) III gotas de solución
muestra 2) III gotas de NaOH-
KOH 2M
4) Observar solución
transparente por
formación de ion
cincato
Frente al NaOH-KOH 2M.
3) Agregar exceso
de reactivo hasta
disolución](https://image.slidesharecdn.com/clase9-cationesg3-2parte-zn-mn-co-ni-150511041726-lva1-app6891/85/Clase-9-cationes-g3-2-parte-zn-mn-co-ni-24-320.jpg)
![Frente al NH3 diluido: NH4OH.
En “ausencia de sales amónicas”
Zn+2 + 2 NH3 + 2 H2O ↔ Zn(OH)2 ↓ blanco/gelatinoso + 2 NH4
+
Zn(OH)2 ↓ + exceso 4 NH3 ↔ [Zn(NH3)4]++/incoloro + 2 OH–
En “presencia sales amónicas”
Zn++ + 4 NH3 ↔ [Zn(NH3)4]++ / incoloro
1) III gotas de solución
muestra
2) II gotas de NH4OH
3M
3) Añadir exceso de
reactivo
INICIALMENTE
CON EXCESO
DE REACTIVO
TÉCNICA](https://image.slidesharecdn.com/clase9-cationesg3-2parte-zn-mn-co-ni-150511041726-lva1-app6891/85/Clase-9-cationes-g3-2-parte-zn-mn-co-ni-25-320.jpg)
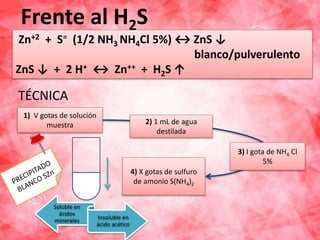
![FRENTE AL FERROCIANURO DE POTASIO 0.5 M.
1) III gotas de solución
muestra
2) 1 mL de agua
destilada
3) III-V gotas de
Fe(CN)6K4 0.5 M.
5) Lavar con 3 mL de
agua destilada, agitar,
centrifugar y observar
TÉCNICA
𝟐𝐙𝐧+𝟐
+ 𝐅𝐞 (𝐂𝐍)𝟔==
⇄ 𝐅𝐞(𝐂𝐍)𝟔𝐙𝐧𝟐 ↓ 𝐛𝐥𝐚𝐧𝐜𝐨.
𝐅𝐞 (𝐂𝐍)𝟔𝐙𝐧𝟐 ↓ +
𝟖 𝑶𝑯
𝑵𝒂𝑶𝑯
−
⇄ 𝟐[𝐙𝐧 (𝐎𝐇)𝟒]=
+ 𝐙𝐧 (𝐂𝐍)𝟔==
4) agitar, centrifugar,
descartar liquido
sobrenadante
SOLUBLE EN HIDRÓXIDO
FUERTEION CINCATO](https://image.slidesharecdn.com/clase9-cationesg3-2parte-zn-mn-co-ni-150511041726-lva1-app6891/85/Clase-9-cationes-g3-2-parte-zn-mn-co-ni-27-320.jpg)