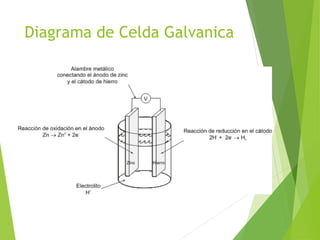
Este documento describe diferentes tipos de corrosión, incluyendo corrosión uniforme, corrosión atmosférica, y corrosión galvánica. La corrosión uniforme ocurre de manera pareja en toda la superficie metálica expuesta a elementos como oxígeno, agua, y contaminantes. La corrosión atmosférica depende de factores como humedad, temperatura y contaminantes en el ambiente. La corrosión galvánica ocurre cuando dos metales de diferente potencial de corrosión entran en contacto en presencia