Enfermedades autosómicas dominantes
- 1. ENFERMEDADES AUTOSÓMICAS DOMINANTES Dulce Álvarez Nieva Hugo González Martínez Montserrat It Morales Alejandra Juárez Daniel Alejandra Lozada Soriano Anette Ana Terán
- 2. Una enfermedad es dominante cuando existe un gen defectuoso (de las dos copias que posee un individuo, la paterna y la materna) y causa los síntomas de alguna enfermedad. El alelo se pudo haber transmitido tanto del padre como de la madre, con una probabilidad para el hijo o hija del 50% de tener o no la enfermedad.
- 3. El patrón de herencia autosómica dominante se da cuando el alelo alterado es dominante sobre el normal y basta una sola copia para que se exprese la enfermedad. Al ser autosómico, el gen se encuentra en uno de los 22 pares de cromosomas no sexuales, o autosomas, pudiendo afectar con igual probabilidad a hijos e hijas.
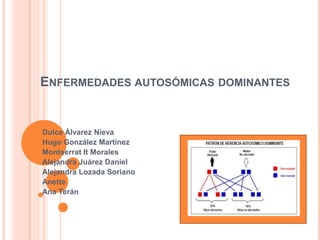
- 4. Patrón de herencia autosómica dominante con un progenitor afectado (azul).
- 5. En estos casos, las anomalías generalmente aparecen en cada generación y cada niño afectado tiene un padre igualmente afectado. Las personas no afectadas no transmiten la enfermedad. Cuando en una familia aparece por primera vez este tipo de herencia es por neomutación. Al elaborar un árbol genealógico de una enfermedad sospechosa de tener un patrón autosómico dominante, debemos tener en cuenta la penetrancia, la expresividad y la edad de aparición del trastorno
- 6. Penetrancia: Porcentaje de individuos con un genotipo dado, que muestran el fenotipo correspondiente. (Un individuo puede tener un genotipo particular y no expresar el fenotipo que se espera de tal genotipo. Ello puede deberse a la presencia en el genoma de otros genes modificadores, genes epistáticos o supresores, o por el efecto del medio ambiente). Expresividad: Describe el grado o la intensidad con que se expresa un genotipo determinado en un individuo. (La falta de expresión completa puede deberse al resto del genoma o factores ambientales)
- 7. ENFERMEDADES AUTOSÓMICAS DOMINANTES FRECUENTES Síndrome de Marfán Acondroplasia Enfermedad de Huntington Neurofibromatosis Enfermedad de Apert Enfermedad de Charcot- Marie- Tooth Enfermedad de Bourneville
- 9. Conocida como neuropatía hereditaria motora y sensitiva o atrofia muscular del peroneo, abarca un grupo de trastornos que afectan los nervios periféricos. Los trastornos que afectan los nervios periféricos se llaman neuropatías periféricas. Afecta aproximadamente a 1 de cada 2.500 personas en los Estados Unidos
- 10. CMT1A: Duplicación de un pequeño segmento del cromosoma 17 que contiene el gen PMP22. Este gen codifica una proteína de la mielina, la PMP-22 la duplicación de este gen presentan 3 copias en lugar de 2, el exceso de copias hace que la función de la mielina se altere y de lugar a una alteración de la función del nervio CMT1B Este tipo se produce por mutaciones del gen MPZ que codifica la proteína cero de la mielina. Las mutaciones de este gen la mayoría de las veces dan lugar a un fenotipo desmielinizante (CMT1B), pero algunas de las mutaciones dan lugar a una forma axonal (CMT2) en estos casos los síntomas clínicos suelen comenzar en la edad adulta.
- 11. CMT2 Son el resultado de la alteración primaria del axón, son menos frecuentes que las formas desmielinizantes y se pueden deber a mutación de muchos genes. Según la literatura la forma CMT2A es la más frecuente y se debe a mutaciones del gen de la mitofusina 2 (MFN2), una proteína que interviene en la función mitocondrial
- 12. CMTX Es una forma de CMT que se transmite de forma dominante ligada al cromosoma X. Esta causada por mutaciones del gen GJB1 que codifica la proteína conexina 32. Mutaciones de este gen dan lugar a una neuropatía que suele cursar con enlentecimiento de la velocidad de conducción en hombres y casi normal o normal en mujeres. En la mayoría de los casos los hombres están mucho más afectados que las mujeres, los síntomas se inician alrededor de la adolescencia con debilidad y atrofia de inicio en piernas y en la eminencia tenar en las manos.
- 13. CARACTERÍSTICAS Debilitaciones en los pies y de los músculos inferiores de la pierna. Deformación del pie como arcos altos y dedos en martillo, genera una marcha a pasos grandes que desencadena en tropiezos o caídas frecuentes. Pérdida de masa muscular en la parte inferior de las piernas.
- 14. DIAGNÓSTICO GENÉTICO El diagnóstico genético es útil para el consejo genético en varias vertientes: Identificar portadores de la enfermedad en caso de que aún no haya signos claros de la misma. Una vez conocida la mutación se puede realizar diagnóstico prenatal y/o preimplantacional. Información de pronóstico en algunos casos. Conocer la historia natural de la enfermedad y tener tipificados a los pacientes para futuros tratamientos.
- 16. Acrocefalosindactilia tipo 1. Pertenece a un grupo de cinco enfermedades caracterizadas, entre otras manifestaciones, por presentar craneosinostosis. Cierre prematuro de las suturas craneales cabeza puntiaguda Deformación de la apariencia de la cara. Cráneo, cara, manos y pies.
- 17. MUTACIÓN EN EL GEN “RECEPTOR 2 DEL FACTOR DE CRECIMIENTO DE FIBROBLASTOS”. Este receptor es fundamental al iniciar los mecanismos moleculares de señalización celular activado por sus ligandos, se produce una cascada de señales dentro de las células que son determinantes a la hora de desencadenar y coordinar los mecanismos inplicados en la fusión ósea alteración o no- regulación de estos mecanismos es la responsable final de la craneosinostosis
- 18. PREVALENCIA Por lo general si los dos miembros de la pareja son sanos, y ya tienen un hijo con síndrome de Apert, existe un riesgo de aproximadamente un 1% de tener un nuevo hijo enfermo. En cambio, y debido a la modalidad de herencia de este síndrome, si una persona afectada quisiera tener un hijo existe un riesgo de un 50% de que pueda heredar dicha enfermedad. 1 - 6 casos por cada 100.000 recién nacidos.
- 23. • Enfermedad autosómica dominante. • Es hereditaria. • Afecta a ambos sexos. • Gen HTT con anomalía en el cromosoma 4. • Defecto genético primario: expresión de un trinucleótido anormal CAG. • Proteína: Huntingtina. • Diagnóstico: PCR. • Tratamiento: no existe
- 24. ACONDROPLASIA
- 25. Es una enfermedad genética, que sigue la herencia clásica propuesta por Mendel. Es autosómica dominante La mutación ocurre en el gen FGFR3 en el locus 4p16.3, lo que confiere una ganancia en la función inhibitoria en el cartílago. La penetrancia es del 100%, su expresividad es limitada . Cursan con talla baja desproporcionada y por lo tanto da la apariencia de macrocefalia (relativa), frente prominente, puente nasal deprimido, torax estrecho, manos en tridente, hiperlordosis y acoramiento rizomelico
- 26. DX desde la 20 SDG Criterios radiológicos : TAC base de cráneo, serie ósea completa con espacios inter pedunculares estrechos, cuerpos vertebrales pequeños, sin diferencia en los distintos niveles, acetábulos planos, crestas iliacas cuadradas y metafisis ensanchadas. Asesoramiento genético: con padres afectados el riesgo de recurrencia es del 50% de un hijo afectado y 50% un hijo sano por embarazo. Por una mutación de novo (90%), el riesgo de recurrencia <1% por embarazo.
- 27. TX: Es paliativo, se les da el seguimiento cada 6 meses se les pide potenciales evocados, se les da hormona de crecimiento sin mejoría significativa. Mujeres miden 125cm, y los Hombres 130cm, orientación nutricional.
- 29. Es una enfermedad autosómica dominante del tejido conjuntivo, que produce afectación multisistémica, sobretodo en esqueleto, los pulmones, los ojos, el corazón y los vasos sanguíneos. Afecta por igual a todos los grupos étnicos. Se calcula que afecta a 1 de cada 5.000 individuos en EE.UU. Los síntomas pueden presentarse desde el nacimiento o aparecer en la edad adulta.
- 30. MODO DE HERENCIA Autosómica dominante; de esta manera, el riesgo de que el hijo de un padre afectado o de una madre afectada tenga la enfermedad es del 50%. Aproximadamente el 75% de los pacientes con SM tiene a uno de sus padres afectado y sólo en un 25% el afectado presenta una mutación de novo (la mutación aparece espontáneamente durante la replicación celular previa a la división celular en el oocito o aparece en un gameto).
- 31. Causado por mutaciones en el gen FBN1, situado en el cromosoma 15 (locus 15q21.1). Este gen es el encargado de producir la proteína fibrilina-1, un componente esencial del tejido conectivo. En el caso de las personas afectadas, esta proteína es escasa o defectuosa y causa una anomalía en la formación del tejido conectivo, formando fibras anormales y menos resistentes. Sin embargo, hay una pequeña proporción de pacientes en los que se han detectado mutaciones en los genes TGFBR 1 y 2 (receptor del factor de crecimiento transformante beta 1 y 2
- 32. MÉTODOS DE ESTUDIO Secuenciación directa de los exones y regiones intrónicas flanqueantes (patrón oro). • DHPLC o cromatografía líquida desnaturalizante de alto rendimiento, con confirmación posterior por secuenciación directa. • Cuando no se identifica una mutación y existe una alta sospecha clínica de la presencia de la enfermedad, pueden buscarse grandes delecciones/duplicaciones (imposibles de detectar por los métodos anteriores) utilizando MLPA (multiplex ligation-dependent probe amplification). • Análisis de ligamiento. Puede ser utilizado para determinar si un individuo ha heredado un alelo del gen FBN1 que está asociado con el síndrome en varios miembros de la familia. Sin embargo, existen limitaciones en familias pequeñas o en presentaciones atípicas de la enfermedad. Además, su coste y su efectividad son limitadas, comparadas con la secuenciación.
- 33. ASPECTOS CLÍNICOS Los pacientes con Síndrome de Marfan presentan incremento de tamaño de huesos largos alteraciones oculares: subluxación o luxación del cristalino que puede acompañarse de miopía intensa, desprendimiento de retina espontáneo Alteraciones cardiovasculares debidas a la debilidad de la capa media de la aorta. El problema más grave asociado con este síndrome es “la debilidad de la aorta”. Cuando esto ocurre, las paredes pueden rasgarse y provocar un derrame de sangre dentro del pecho o abdomen. Si estos derrames son repentinos y de gran magnitud, pueden provocar la muerte.
- 36. Enfermedad de origen genético consistente en el crecimiento de tumores benignos (hamartomas), y malformaciones en uno o varios órganos: piel, cerebro, riñones, corazó n, ojos, pulmones, dientes, e tc. la afectación es muy variable, desde únicamente pequeñas alteraciones cutáneas hasta retraso mental importante y problemas en múltiples órganos “expresividad
- 37. Radica en la alteración de una porción del cromosoma 9 (locus 9q34), del cromosoma 16 (locus 16p13) o del cromosoma 11 (locus 1 lq21). Estos genes contienen información para la síntesis de unas proteínas llamadas “hamartina y tubarina”, que se cree que son inhibidores tumorales. Al ser anómalos esos genes, no se producen los inhibidores y, por tanto, existe tendencia a la aparición de tumores, que suelen ser benignos.
- 38. Cada hijo tiene el 50% de posibilidades de heredar la enfermedad. Sin embargo, a pesar de ser una enfermedad hereditaria, aproximadamente el 60% de los casos son de aparición espontánea, sin que ninguno de los progenitores tengan la enfermedad. Esto se debe a que aparecen nuevas mutaciones, nuevos errores en los genes de las células germinales que formarán el nuevo embrión. Esta enfermedad afecta aproximadamente a uno de cada 6,000 nacidos vivos.
- 39. TÉCNICAS DE DIAGNÓSTICO Estudios de neuroimagen Se realizará ecografia cerebral en caso de ser la fontanela craneal aún permeable. En caso de que no lo sea, se debe hacer una tomografia axial computarizada (TAC), que permite la identificación de nódulos subependimarios, pues detecta bien las calcificaciones. Ecografía Estudios de imagen renal y cardiaca, fondo de ojo Biopsia
- 40. ASPECTOS CLÍNICOS Triada 1. Retraso mental 2. Angiofibrosomas 3. Epilepsia astrocitomas múltiples en la retina tuberocidades corticales angioblastoma facial múltiples nódulos subependimales calcificados que protuyen dentro del ventrículo nódulos subependimales Pueden evolucionar a: tuberosidades croticales; quistes renales; linfangiomatosis pulmonares; hamatoma de retina
- 41. BIBLIOGRAFÍA Ruíz R, Guerra L. Síndrome de Apert. Feaps 2008; cap 10: 277 – 292. Rosales Reynoso Mónica Alejandra. Barros Núñez Patricio. “Diagnostico molecular de la enfermedad de Huntington”. División de Genética, Centro de Investigación Biomédica de Occidente, Instituto Mexicano del Seguro Social, Guadalajara, Jal., México. Recibido en su versión modificada: 17 de septiembre de 2007, Aceptado: 14 de diciembre de 2007. http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S0864-215X2000000100013 4.Loeys BL, Dietz HC, Braverman AC, et-al. The revised Ghent nosology for the Marfan syndrome. J Med Genet. 2010;47:476-85. Medline 5.Arslan-Kirchner M, Arbustini E, Boileau C, et-al. Clinical utility gene card for: Marfan syndrome type 1 and related phenotypes [FBN1]. Eur J Hum Genet. 2010;18. Instituto de Investigación Biomédica de A Coruña (INIBIC)-Complejo Hospitalario Universitario A Coruña (CHUAC), A Coruña, Galicia, España Sainz H.; et al. Esclerosis tuburosa, *Facultad de Educación de la Universidad de Cantabria **Servicio de Pediatría del Hospital Universitario Marques de Valdecilla, pag 313..
