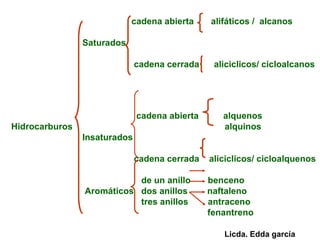
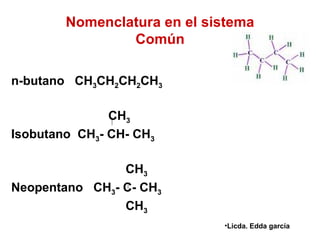
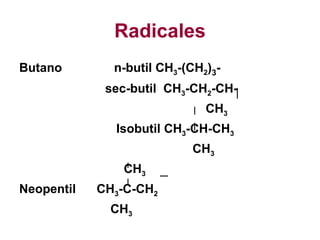
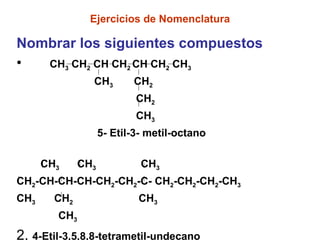
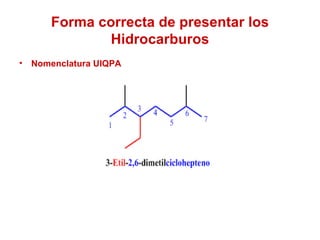
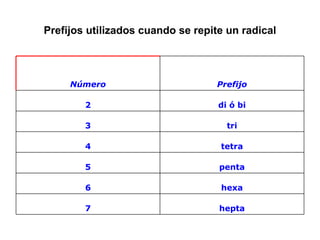
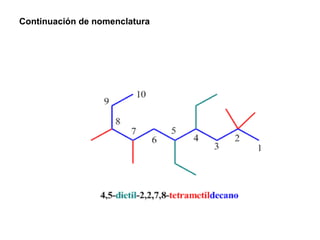
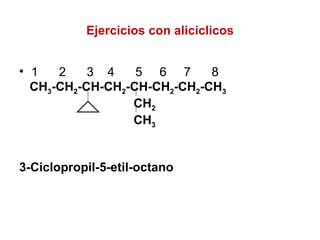
El documento habla sobre los hidrocarburos, compuestos orgánicos formados por carbono e hidrógeno. Menciona que Titán, la luna de Saturno, contiene grandes cantidades de hidrocarburos, suficientes para abastecer la energía mundial por siglos. Luego describe diferentes tipos de hidrocarburos como alifáticos, alquenos, alquinos y aromáticos.