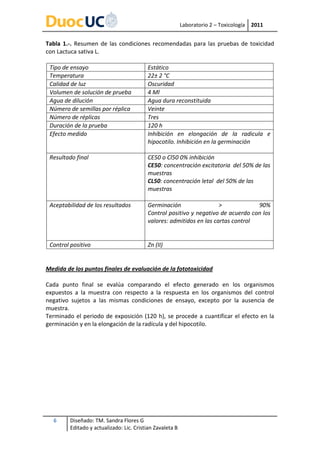
El documento describe un ensayo de toxicidad para evaluar los efectos fitotóxicos del bicromato de potasio (K2CrO4) en semillas de lechuga (Lactuca sativa) mediante la cuantificación de la inhibición en la germinación y elongación de la radícula y el hipocotilo. El ensayo involucra la preparación de soluciones de K2CrO4 a diferentes concentraciones y la incubación de las semillas expuestas durante 120 horas para medir los efectos en el desarrollo de las plántulas. El objetivo