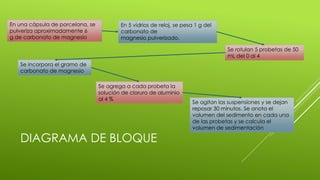
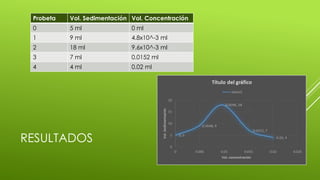
Este documento describe una práctica de laboratorio sobre la floculación controlada de suspensiones mediante electrolitos. Explica que las suspensiones son dispersiones heterogéneas de una fase sólida en una fase líquida y que al agregar soluciones de electrolitos como el cloruro de aluminio a diferentes concentraciones se pueden inducir reacciones de floculación que hacen sedimentar las partículas, midiendo así el volumen de sedimentación en función de la concentración del electrolito.