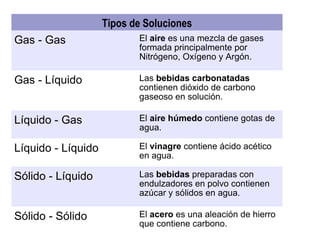
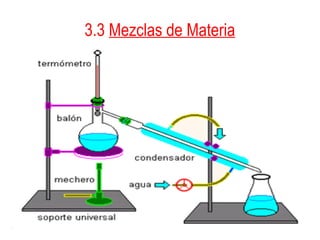
Este documento resume los conceptos clave del Capítulo 3 sobre las propiedades y cambios de la materia. Explica que la materia tiene propiedades físicas y químicas, y puede existir en tres estados: sólido, líquido y gas. También describe los cambios físicos y químicos, la conservación de la masa, y los diferentes tipos de mezclas y métodos para separarlas, como filtración, destilación, cristalización y cromatografía.