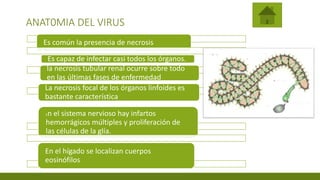
El virus de Marburgo presenta una estructura típica de filovirus con una nucleocápside que contiene ARN de polaridad negativa envuelta en una envoltura viral. Se contagia principalmente por contacto cercano con fluidos corporales infectados y causa una patogénesis mediada por macrófagos que dañan las células endoteliales. El diagnóstico se basa en el aislamiento viral, detección de anticuerpos o material genético, mientras que el tratamiento consiste principalmente en terapia de soporte.