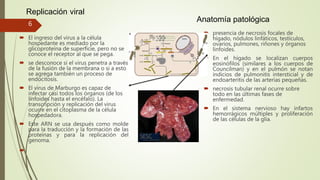
El documento describe la historia, estructura y replicación del virus de Marburgo. El virus fue aislado por primera vez en 1967 en Alemania tras una epidemia entre trabajadores de laboratorio. Desde entonces ha habido varios brotes, incluyendo uno grande en Angola en 2004 que causó 374 casos y 329 muertes. El virus tiene forma de bastoncillo y contiene ARN negativo envuelto en una envoltura lipídica. Se replica en el citoplasma de la célula huésped y puede infectar muchos órganos. No existe una vacuna a