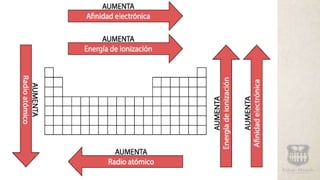
El documento describe las propiedades periódicas de los elementos, incluyendo cómo varían el radio atómico, la energía de ionización, la afinidad electrónica y la electronegatividad a través de la tabla periódica. Explica que estas propiedades dependen de la configuración electrónica y cómo aumentan o disminuyen al moverse a través de los períodos y grupos. También incluye preguntas sobre cómo aplicar el conocimiento de las variaciones de las propiedades periódicas.