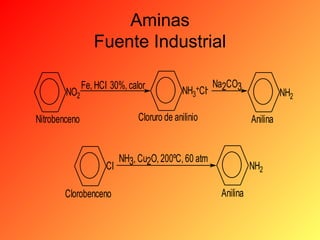
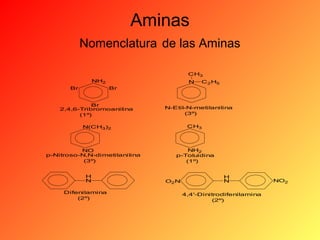
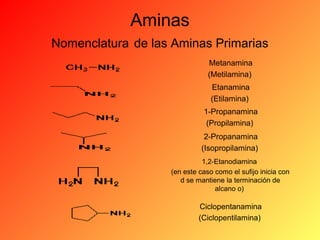
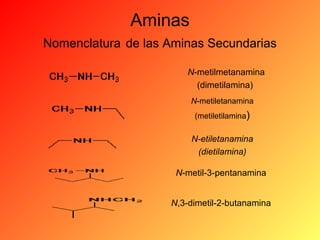
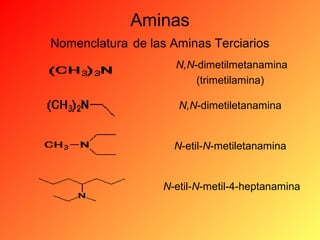
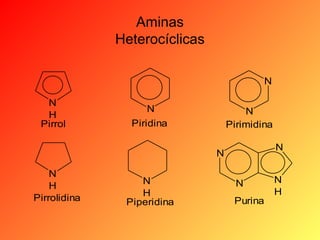
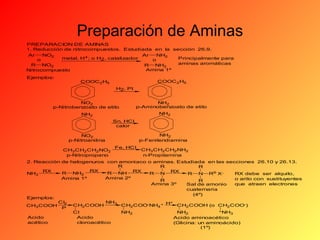
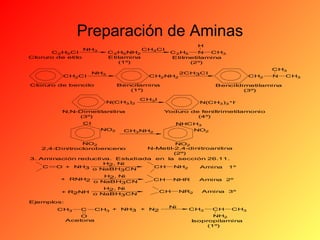
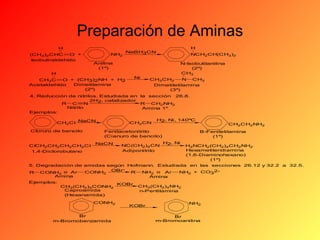
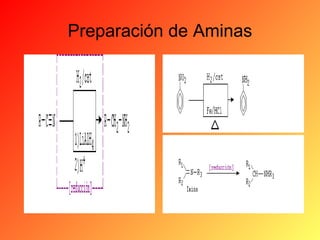
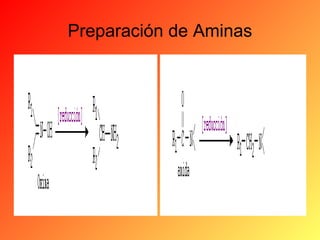
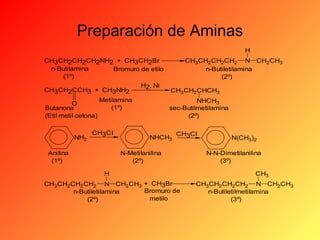
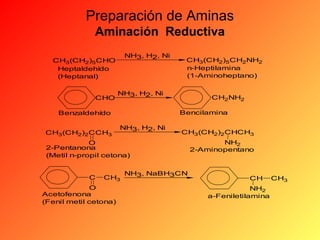
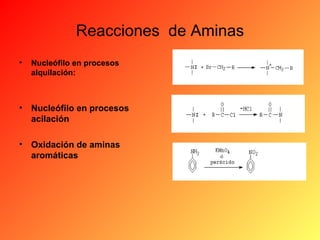
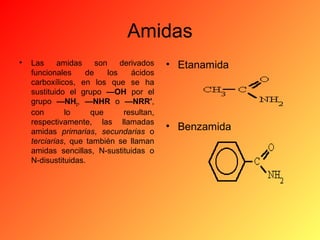
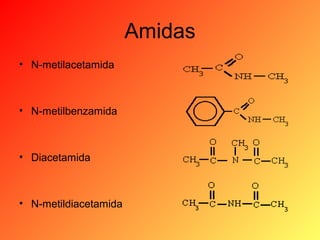
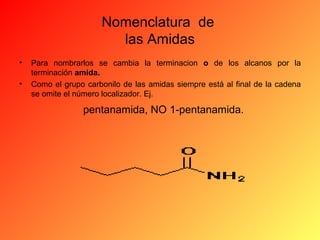
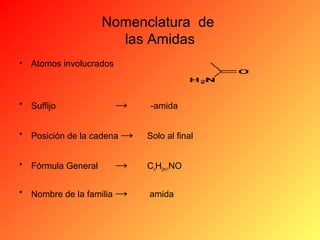
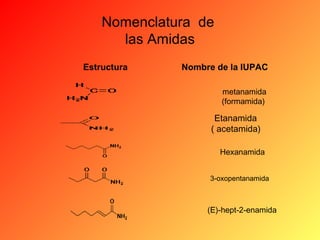
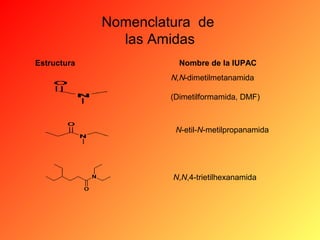
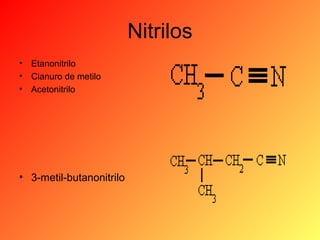
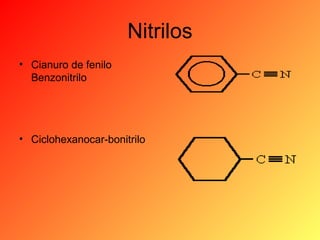
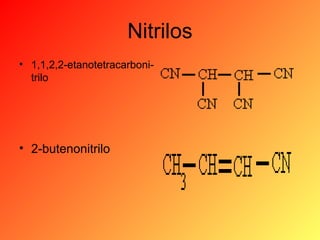
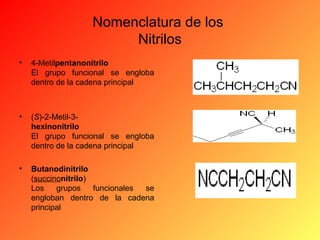
Este documento proporciona información sobre el tema de química orgánica de aminas, amidas y nitrilos impartido por el Ing. Miguel Hurtado Gastañadui. El documento incluye una lista de estudiantes y detalla las propiedades, clasificación, estructura, nomenclatura y fuentes industriales de las aminas. También cubre aminas heterocíclicas como la piridina y la piperidina.