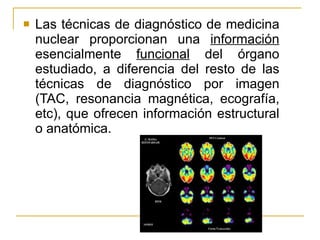
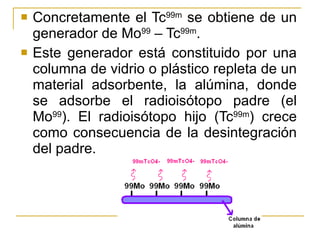
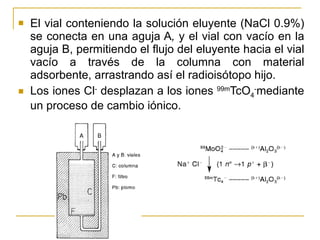
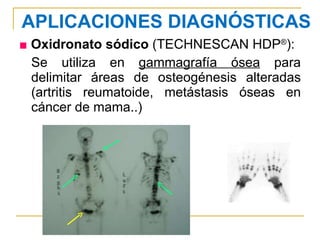
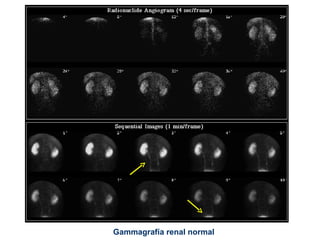
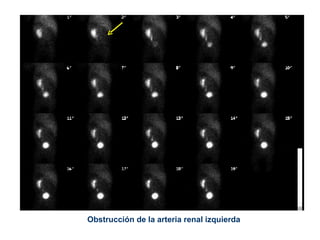
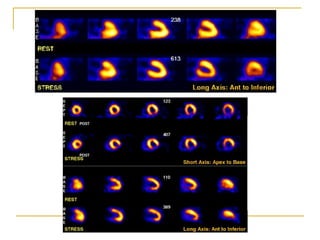
El documento define la radiofarmacia como la especialidad que estudia los aspectos farmacéuticos, químicos y biológicos de los radiofármacos y aplica estos conocimientos en su diseño, producción, preparación y uso. Explica que un radiofármaco contiene un radionucleido que emite radiación para diagnóstico o tratamiento y una molécula que se dirige a un tejido u órgano específico. También describe los procesos de obtención del tecnecio 99m, el isótopo más utilizado