Revista quimica camila anzola 4 to b
- 2. Los enlaces químicos pág. 3 Electrones de valencia pág. 4 Tipos de enlaces pág. 5 Naturaleza del enlace covalente pág. 6 Polaridad de enlaces covalentes pág. 7 Anuncios pág. 8 Estructura de Lewis pág. 9 Excepciones de la ley del octeto pág. 10 Electronegatividad pág. 11 Crucigrama pág. 12 Publicidad pág. 13
- 3. Los enlaces químicos Un enlace químico es la unión entre dos o más átomos para formar una entidad de orden superior, como una molécula o una estructura cristalina. El compuesto que resulta de este enlace es químicamente y físicamente único y diferente de sus átomos originarios.La formación de enlaces se produce siempre por un balance favorable de energía, es decir, los átomos enlazados constituyen un sistema de menos energía que los átomos por separado. Ejemplo Pág. 3
- 4. Electrones de valencia Los electrones de valencia son cualquiera de las partículas que se encuentran cargadas de forma negativa y que son fundamentales en la región más externa de los átomos la cual participa de forma activa en la formación de los diferentes enlaces químicos. Cuáles son los electrones de valencia Los electrones de valencia son aquellos electrones que se encuentran ubicados en la capa más externa de un átomo y son los encargados de realizar la interacción de cada elemento con otros para poder formar enlaces, y de la estabilidad y fuerza de estos. El lugar donde se encuentran ubicados los electrones de valencia corresponde al último nivel del átomo. O más bien lo que sería el orbital más lejano. Ejemplos •Cobre: el cobre posee únicamente 2. •Flúor: tiene 7. •Argón: posee 8 en su último nivel. Pág. 4
- 5. Es la unión de dos átomos mediante la compartición de dos electrones de sus correspondientes capas de valencia. Una vez compartidos, los electrones no pertenecen en forma exclusiva a ninguno de los átomos, y se encuentran localizados en el espacio intranuclear de los mismos. • Enlace iónico: Debido a la atracción electrostática entre iones. Típico de la combinación de elementos metálicos con elementos no metálicos. • Enlace covalente. • Enlace metálico. Debido a la compartición de electrones de forma colectiva. Típico de los elementos metálicos. Pág. 5
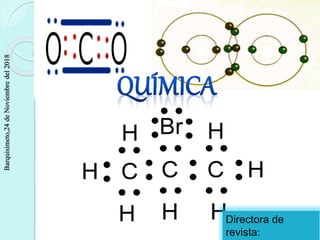
- 6. Naturaleza del enlace covalente Enlace covalente simple: Cada átomo aporta un electrón al enlace, es decir, se comparte un par de electrones entre dos átomos. Un ejemplo es la molécula de Hidrógeno (H2): Otro ejemplo de este tipo de enlace sería la molécula de cloro Enlace covalente doble: Cada átomo aporta dos electrones al enlace, es decir, se comparten dos pares de electrones entre dos átomos. Un ejemplo es la molécula de Oxígeno (O2): Enlace covalente triple: Cada átomo aporta tres electrones al enlace, es decir, se comparten tres pares de electrones entre dos átomos, por ejemplo, la molécula de Nitrógeno (N2). Pág. 6
- 7. Enlace covalente polar Enlace covalente no polar Se forma entre átomos iguales y la diferencia de electronegatividad debe ser cero o muy disminuida (menor que 0,4). En este enlace, los electrones son atraídos por ambos núcleos con la misma intensidad, generando moléculas cuya nube electrónica es uniforme. Consiste en la formación de un enlace entre átomos de diferentes elementos, y la diferencia de la electronegatividad debe ser mayor de 0,4. En este enlace, los electrones son atraídos fundamentalmente por el núcleo del átomo más electronegativo, generando moléculas cuya nube electrónica presentará una zona con mayor densidad de carga negativa y otra con mayor densidad de carga positiva (dipolo). Tolueno Fenol Pág. 7
- 8. Pág. 8
- 9. Esta representación se usa para saber la cantidad de electrones de valencia de un elemento que interactúan con otros o entre su misma especie, formando enlaces ya sea simples, dobles, o triples y estos se encuentran íntimamente en relación con los enlaces químicos entre las moléculas y su geometría molecular, y la distancia que hay entre cada enlace formado. también llamada diagrama de punto, modelo de Lewis o representación de Lewis, es una representación gráfica que muestra los enlaces entre los átomos de una molécula y los pares de electrones solitarios que puedan existir. Pág. 9
- 10. Berilio (Be) Es una excepción a la regla del Octeto porque es capaz de formar compuestos con dos enlaces simples, siendo así, se estabiliza con apenas cuatro electrones en la capa de valencia. Como el hidrógeno (H) precisa ceder dos electrones para realizar el enlace (H ― Be ― H), el átomo de Berilio (Be) comparte sus electrones y alcanza la estabilidad. Aluminio (Al) Es una excepción a la regla del octeto porque alcanza la estabilidad con seis electrones en la capa de valencia. El átomo de aluminio tiende a donar sus electrones y así puede formar tres enlaces simples con otros átomos. En este caso, el Aluminio (Al) formó tres enlaces con tres átomos de Fluor (F) Boro (B) Forma sustancias moleculares con tres enlaces simples. Fijémonos que el Boro (B) tiene la tendencia de donar sus electrones para los átomos de Flúor (F), este si obedece a la regla del Octeto, necesitando sus ocho electrones en la capa de valencia. Como el Boro cede sus electrones, el Flúor se estabiliza con el Octeto formado. Pág. 10
- 11. Pauling la definió como la capacidad de un átomo en una molécula para atraer electrones hacia así. Sus valores, basados en datos termoquímicos, han sido determinados en una escala arbitraria, denominada escala de Pauling, cuyo valor máximo es 4 que es el valor asignado al flúor, el elemento más electronegativo. El elemento menos electronegativo, el cesio, tiene una electronegatividad de 0,7. La electronegatividad de un elemento mide su tendencia a atraer hacia sí electrones, cuando está químicamente combinado con otro átomo. Cuanto mayor sea, mayor será su capacidad para atraerlos. Pág. 11
- 12. Pág. 12
- 13. Pág. 13