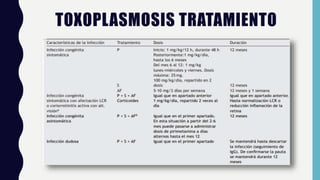
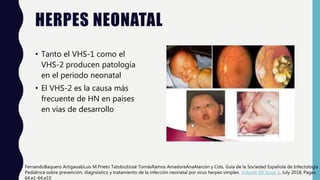
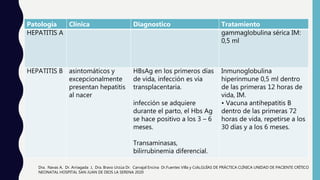
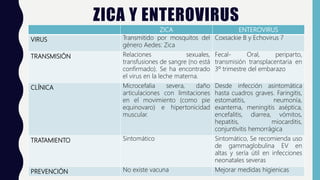
El documento resume las principales características de las infecciones TORCH. Describe brevemente cada una de las infecciones (toxoplasmosis, rubeola, citomegalovirus, herpes y sífilis) incluyendo su ciclo de vida, manifestaciones clínicas, diagnóstico y tratamiento. Se enfoca en las infecciones congénitas y la importancia del diagnóstico y tratamiento oportuno para prevenir secuelas en el feto y recién nacido.