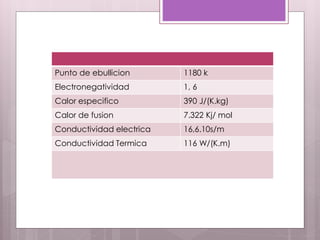
El documento proporciona información sobre las propiedades y funciones del zinc. Explica que el zinc es un metal de transición esencial para la salud humana. Se encuentra naturalmente en los alimentos y desempeña un papel importante en más de 300 enzimas y 3000 proteínas del cuerpo. La deficiencia de zinc puede provocar retraso en el crecimiento, alteraciones óseas y dermatitis, entre otros problemas. Industrialmente, el zinc se usa principalmente para proteger otros metales de la corrosión.




![Radio atomico 142
Radio covalente 131 pm
Configuracion electronica [Ar]3𝑑10, 4𝑠2
Electrones por capa 2, 8, 18, 2
Estados de oxidacion 2
Oxido Anfotero
Estructura cristalina Hexagonal
Estado Solido
Punto de fusion 692.68 K](https://image.slidesharecdn.com/zinc-140605183239-phpapp01/85/Zinc-5-320.jpg)