Grado de oxidación
•Descargar como DOCX, PDF•
0 recomendaciones•2,986 vistas
Estan las valencias y cxomo se forman la nomenclatura inórganica.
Denunciar
Compartir
Denunciar
Compartir
Recomendados
Más contenido relacionado
La actualidad más candente
La actualidad más candente (20)
Tabla periódica con los número de oxidación de los elementos más comunes

Tabla periódica con los número de oxidación de los elementos más comunes
Ejercicios con-resoluci--n-ii-----qu--mica-org--nica--gratis-

Ejercicios con-resoluci--n-ii-----qu--mica-org--nica--gratis-
Similar a Grado de oxidación
Similar a Grado de oxidación (13)
Más de Alumic S.A
Más de Alumic S.A (20)
Último
Último (20)
La empresa sostenible: Principales Características, Barreras para su Avance y...

La empresa sostenible: Principales Características, Barreras para su Avance y...
MAYO 1 PROYECTO día de la madre el amor más grande

MAYO 1 PROYECTO día de la madre el amor más grande
Lecciones 05 Esc. Sabática. Fe contra todo pronóstico.

Lecciones 05 Esc. Sabática. Fe contra todo pronóstico.
PIAR v 015. 2024 Plan Individual de ajustes razonables

PIAR v 015. 2024 Plan Individual de ajustes razonables
LABERINTOS DE DISCIPLINAS DEL PENTATLÓN OLÍMPICO MODERNO. Por JAVIER SOLIS NO...

LABERINTOS DE DISCIPLINAS DEL PENTATLÓN OLÍMPICO MODERNO. Por JAVIER SOLIS NO...
ACERTIJO DE LA BANDERA OLÍMPICA CON ECUACIONES DE LA CIRCUNFERENCIA. Por JAVI...

ACERTIJO DE LA BANDERA OLÍMPICA CON ECUACIONES DE LA CIRCUNFERENCIA. Por JAVI...
Curso = Metodos Tecnicas y Modelos de Enseñanza.pdf

Curso = Metodos Tecnicas y Modelos de Enseñanza.pdf
Programacion Anual Matemática4 MPG 2024 Ccesa007.pdf

Programacion Anual Matemática4 MPG 2024 Ccesa007.pdf
proyecto de mayo inicial 5 añitos aprender es bueno para tu niño

proyecto de mayo inicial 5 añitos aprender es bueno para tu niño
plande accion dl aula de innovación pedagogica 2024.pdf

plande accion dl aula de innovación pedagogica 2024.pdf
Grado de oxidación
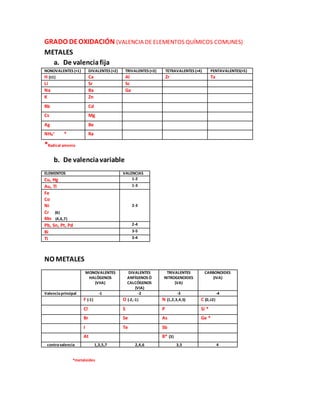
- 1. GRADO DEOXIDACIÓN (VALENCIA DE ELEMENTOS QUÍMICOS COMUNES) METALES a. De valenciafija NONOVALENTES (+1) DIVALENTES (+2) TRIVALENTES (+3) TETRAVALENTES (+4) PENTAVALENTES(+5) H (±1) Ca Al Zr Ta Li Sr Sc Na Ba Ga K Zn Rb Cd Cs Mg Ag Be NH4 + * Ra *Radical amonio b. De valenciavariable ELEMENTOS VALENCIAS Cu, Hg 1-2 Au, Tl 1-3 Fe Co Ni Cr (6) Mn (4,6,7) 2-3 Pb, Sn, Pt, Pd 2-4 Bi 3-5 Ti 3-4 NO METALES MONOVALENTES HALÓGENOS (VIIA) DIVALENTES ANFÍGENOS Ó CALCÓGENOS (VIA) TRIVALENTES NITROGENOIDES (VA) CARBONOIDES (IVA) Valenciaprincipal -1 -2 -3 -4 F (-1) O (-2,-1) N (1,2,3,4,5) C (0,±2) Cl S P Si * Br Se As Ge * I Te Sb At B* (3) contravalencia 1,3,5,7 2,4,6 3,5 4 *metaloides
- 2. FORMACIÓN DE COMPUESTOS BINARIOS 1. ÓXIDOS METÁLICOS = METAL + OXÍGENO (ÓXIDOSBÁSICOS) 2. ÓXIDOS NO METÁLICOS = NO METAL + OXÍGENO (ÓXIDOSÁCIDOSU ANHÍDRIDOS) 3. PERÓXIDOS = ÓXIDOS(I-II) +OXÍGENO(-1) 4. ÓXIDOS SALINOS = SUMA DE 2 ÓXIDOSDEL MISMO METAL DE VAL.VARIABLE2,3 5. ÁCIDOS HIDRÁCIDOS = HIDRÓGENO + NO METAL (VI-VII) (HIDRUROSNO METÁLICOS) 6. COMPUESTOSESPECIALES= HIDRÓGENO+ NO METAL(IV-V) 7. HIDRUROS METÁLICOS = METAL + HIDRÓGENO 8. HALUROS METÁLICOS = METAL + NOMETAL(IV-V) (COMPUESTOSSALINOS) 9. HALUROS NO METÁLICOS= NOMETAL (+ELECTRO-) + NOMETAL (-ELECTRO-) (COMPUESTOSNO SALINOS) 10. AMALGAMASBINARIAS= METAL + MERCURIO (MEZCLA) 11. ALEACIONES BINARIAS = METAL + METAL (MEZCLA) 12. SALES HALÓGENAS NEUTRAS = HIDRÓXIDO+ ÁCIDOHIDRÁCIDO FORMACIÓNDE COMPUESTOSTERNARIOS 1. HIDÓXIDOS = OXIDOBASICO+ AGUA (BASEINORGANICA) 2. ACIDO OXACIDOS = OXIDOÁCIDO+ AGUA (ANHÍDRIDO) FORMACIÓNDIRECTA DE SALES 1. SAL HALÓGENA NEUTRA = METAL + RADICALHIDRÁCIDO 2. SAL OXISAL NEUTRA = METAL + RADICALOXÁCIDO 3. SAL HALÓGENA ÁCIDA = METAL + (HIDRÓGENO+RADICALHIDRÁCIDOVIA) 4. SAL OXISAL ÁCIDA = METAL + (HIDRÓGENO+RADICALOXÁCIDODEVAL2 O MAS)
