Grupos funcionales 1 1 1 1 1
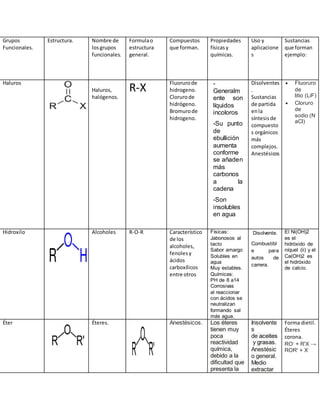
- 1. Grupos Funcionales. Estructura. Nombre de losgrupos funcionales. Formulao estructura general. Compuestos que forman. Propiedades físicasy químicas. Uso y aplicacione s Sustancias que forman ejemplo: Haluros Haluros, halógenos. R-X Fluorurode hidrogeno. Clorurode hidrógeno. Bromurode hidrogeno. - Generalm ente son líquidos incoloros -Su punto de ebullición aumenta conforme se añaden más carbonos a la cadena -Son insolubles en agua Disolventes . Sustancias de partida enla síntesisde compuesto s orgánicos más complejos. Anestésicos Fluoruro de litio (LiF) Cloruro de sodio (N aCl) Hidroxilo Alcoholes R-O-R Característico de los alcoholes, fenolesy ácidos carboxílicos entre otros Físicas: Jabonosos al tacto Sabor amargo Solubles en agua Muy estables. Químicas: PH de 8 a14 Corrosivas al reaccionar con ácidos se neutralizan formando sal más agua. Disolvente. Combustibl e para autos de carrera. El Ni(OH)2 es el hidróxido de níquel (ii) y el Ca(OH)2 es el hidróxido de calcio. Éter Éteres. Anestésicos. Los éteres tienen muy poca reactividad química, debido a la dificultad que presenta la Insolvente s de aceites y grasas. Anestésic o general. Medio extractar Forma dietil. Éteres corona. RO- + R'X → ROR' + X-
- 2. ruptura del enlace C— O. Estructuralm ente los éteres pueden considerarse derivados del agua o alcoholes. para concentrar ácido acético y otros ácidos. Carbonilo. carbonilo Aldehído. Cetona. Ácido carboxílico. Éster. l grupo carbonilo presenta hibridación sp2 en el carbono por lo que es plana. Por su polaridad los aldehídos Por su polaridad dirigida hacia su oxigeno causa un carbono electrofónico que es capaz de aceptar nucleótidos. Remoción de impurezas que le dan color, olor y sabor al agua potable Proceso de descafeinad o del café Decoloraci ón de azúcar, mieles, caramelos … Reducci ón de Wolff- Kishner Reducci ón de Clemme nsen Convers ión en tioac etales Cetona. carbonilo La acetona para despintar lasuñas. Las cetonas en compuestos polares. Los puntos de ebullición son mayores que el de los alcanos del mismo peso molecular. Se comportan como ácidos debido a la presencia del grupo carbonilo. .-Síntesis de medicamen tos .-Síntesis de vitaminas .-Aplicación en cosméticos .Adhesivos en base de poliuretano.
- 3. Carboxilo Ácidos carboxílicos. Estos ácidos son los que nos permiten apreciar la sensación agridulce cuando tomamos una limonada, el sabor especial de la vinagreta en una ensalada, o los agradables olores de las frutas frescas. Los ácidos carboxílicos forman sales metálicas en las reacciones acido base. Tienen un olor fuerte parecido al de la mantequilla rancia y el sudor de cabra. Se utilizan los ácidos carboxílic os como emulsifica ntes, se usan especialm ente para pH bajos, debido a su estabilida d en estas condicione s. Ester Esteres Ésteres orgánicos: Son los que tienen un alcohol y un ácido orgánico. Como ejemplo basta ver el etanoato de propilo expuesto arriba. Ésteres inorgánicos: Son los que derivan de un alcohol y de un ácido inorgánico. Aislantes eléctricos en fusión y en disolución. Bajo temperatura de fusión y ebullición que crece con la masa molar. En las reacciones de esteres la cadena se siempre rompe en un enlace sencillo. Los esteres se utilizan como saboresy fragancias artificiales, debidoasu característi co aroma. Aminas amino Son la morfina y la nicotina. Algunas aminas son biológicame nte importantes como la Estructura molecular los átomos de nitrógeno en amonasposee un hibridismo ap3 y dos electrones despegados por lo que estos compuestos presentan una Las aminas son empleadas para la elaboración de caucho sintéticoy colorante.
- 4. adrenalina y la noradrenali na. estructura tetragonal. Son muysolubles. Amidas Aminoy carbonilo Compuestos orgánicosque pueden considerase derivadosde ácidoso aminas,se derivande los ácidos carboxílicos alifáticoso aromáticos, Así como de otros tiposde ácidos,como losque contienen azufre o fósforo. Casi todas las amidas son incoloras e inodoras Son neutras frente a los indicadores. Las amidas son solo muy débilmente básicas, debido a la interacción mesómera entre el Doble enlace carboxílico y el par de electrones del átomo de nitrógeno. Como emu lsificantes, se usan especialme nte para pH baj os, debido a su estabilidad en estas condiciones . Además se usan como antitranspir ante y como neutralizant es... Otra aplicación es como dispersante s de jabones cálcicos.