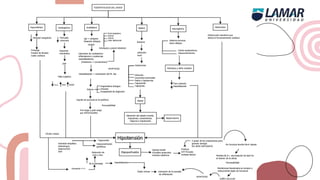
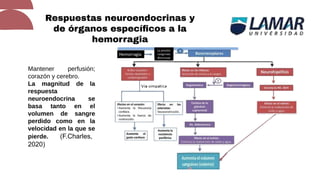
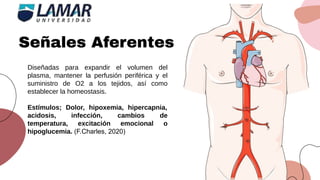
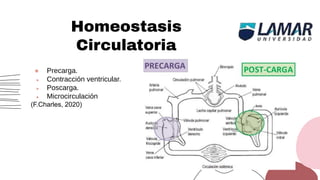
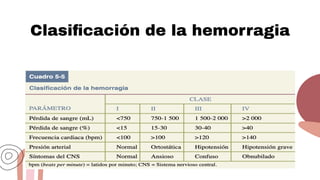
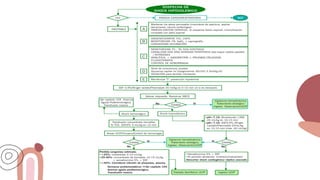
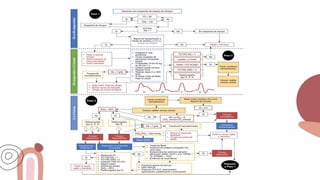
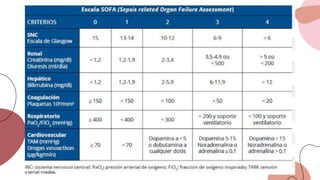
Este documento trata sobre el choque. Resume las causas, manifestaciones clínicas, respuestas fisiológicas y procesos inflamatorios asociados con el choque, así como los diferentes tipos de choque como el hipovolémico. Explica conceptos como hipoperfusión celular, respuestas neuroendocrinas, citocinas, complemento y señalización celular durante el estado de choque.