Incrustar presentación
Descargado 59 veces


![[O 2 ] -2 Ca +2 Ca [O 2 ] Ca O 2 Na +1 [O 2 ] -2 Na 2 [O 2 ] Na 2 O 2 NO SE PUEDEN SIMPLICAR LOS SUBINDICES ¿Cuántas cargas negativas se necesitan para que el compuesto sea neutro eléctricamente?](https://image.slidesharecdn.com/3-perxidos-100418053057-phpapp02/85/3-peroxidos-3-320.jpg)
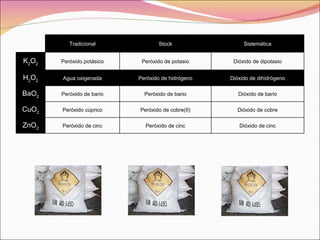

Este documento describe los peróxidos, compuestos formados por la unión del oxígeno consigo mismo en el grupo peróxido. Explica que en estos compuestos el oxígeno tiene un número de oxidación de -1 y que para que sean eléctricamente neutros se necesitan la cantidad adecuada de cargas negativas. Además, lista ejemplos comunes de peróxidos y explica por qué no pueden simplificarse a óxidos.


![[O 2 ] -2 Ca +2 Ca [O 2 ] Ca O 2 Na +1 [O 2 ] -2 Na 2 [O 2 ] Na 2 O 2 NO SE PUEDEN SIMPLICAR LOS SUBINDICES ¿Cuántas cargas negativas se necesitan para que el compuesto sea neutro eléctricamente?](https://image.slidesharecdn.com/3-perxidos-100418053057-phpapp02/85/3-peroxidos-3-320.jpg)

