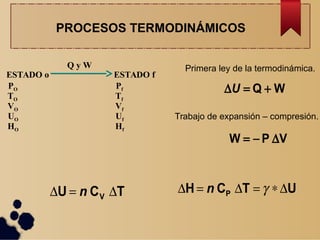
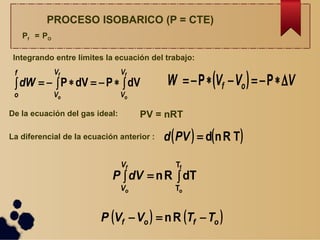
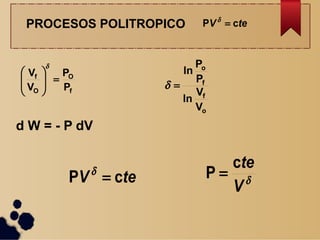
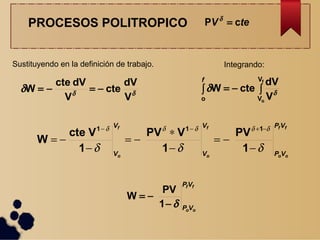
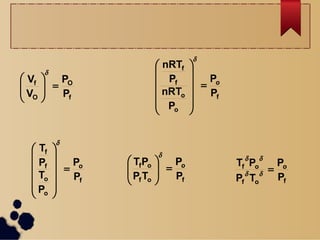
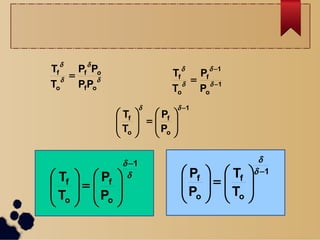
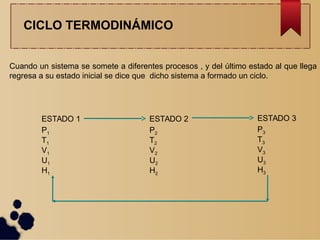
Este documento describe los diferentes procesos termodinámicos como isotérmicos, isobáricos, isocóricos y adiabáticos. Explica las ecuaciones que rigen cada proceso y cómo calcular el trabajo y la transferencia de calor. También define los ciclos termodinámicos y las máquinas térmicas y de refrigeración, incluida su eficiencia y coeficiente de rendimiento.