Diapositivas de ph quimica
- 1. PH
- 2. El termino de pH procede del latín. Quiere decir pondus hydrogenii peso de hidrogeno. Otra posible explicación del significado es potentina hydrogenii= efectividad del hidrogeno. El valor de pH tiene un papel importante en la industria, la medicina, en el sector de alimentación y en la agricultura. Se mide sobre todo en soluciones acuosas, extractos, pero también en productos con consistencia solida(eje; frutas) o también en el cuerpo humano(eje; valor de pH de la piel).también es importante que para hacer posible una medición correcta debe darse una humedad suficiente del objeto medio. El valor pH se determina por medio de indicadores o con aparatos de medición digitales. Los indicadores de sustancias colorantes que cambia su color en un rango de pH determinado. según la definición química, el valor de pH es el logaritmo negativo en décadas del valor numérico de la actividad molar de los iones de hidrogeno ah+: PH= -lgah+ La soluciones con un pH inferior a 7 reaccionan de manera acida, con un valor de pH de 7 son neutras. En soluciones con un pH a 7 reaccionan de manera básica. PH
- 3. El POH se define como el logaritmo negativo de la actividad de los iones de hidróxido. Esto es, la concentración de iones OH-: POH= − log10.[OH − ] En soluciones acuosas, los iones OH- provienen de la disociación del agua: H2O ↔ H+ + OH- o también, 2H2O ↔ H3O+ + OH- Por ejemplo, una concentración de [OH-] = 1×10-7 M (0,0000001 M) es simplemente un POH de 7 ya que : POH = -log[10-7] = 7 Al igual que el pH, típicamente tiene un valor entre 0 y 14 en disolución acuosa, siendo ácidas las disoluciones con POH mayores a 7, y básicas las que tienen POH menores a 7. Por lo tanto, pH + POH = 14 POH
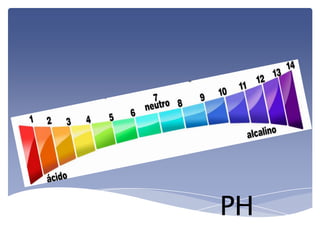
- 4. La escala de pH típicamente va de 0 a 14 en disolución acuosa, siendo ácidas las disoluciones con pH menores a 7 (el valor del exponente de la concentración es mayor, porque hay más iones en la disolución) y alcalinas las que tienen pH mayores a 7. El pH = 7 indica la neutralidad de la disolución (cuando el disolvente es agua). ESCALA DEL PH
- 5. Es importante tener conocimiento sobre el pH en nuestros alimentos(acidez) ya que si ingerimos alimentos ácidos esto podría provocar alteraciones en nuestro organismo. el PH en nuestros alimentos
- 6. Para medir el pH de una disolución podemos emplear dos métodos, en función de la precisión con que queramos hacer la medida: Para realizar medidas del pH que no necesiten ser muy precisas se utilizan unas sustancias llamadas indicadores, que varían reversiblemente de color en función del pH del medio en que están disueltas. Se pueden añadir directamente a la disolución o utilizarlas en forma de tiras de papel indicador (tabla inferior). Para realizar medidas exactas se utiliza un pH-metro, que mide el pH ( la tabla inferior) por un método potencio métrico. INDICADOR EN DISOLUCION PAPEL INDICADOR PH- METRO COMO SE PUEDE MEDIR EL PH?
- 7. Jugo de repollo morado En general se les denomina: Antocianinas, porque son varias. El repollo morado o col lombarda contiene en más porcentaje la cianidina correspondiente. Se manifiesta con un color rojo a pH ácidos menores a 6,5 y morada encima de 6,5. Se vuelve azul encima de 7,5. El efecto se produce por una modificación de la estructura del grupo flavilo(es decir el 2-fenil-benzopirilio) por formar un anillo por causa de la presencias del H (+) es decir ácidos, que se abrió en pH básicos (por ejemplo agua con jabón). La presencia prolongada de bases destruye por completo la disposición básica del grupo flavilo, por consiguiente, el color desaparece. Sustancias para medir el pH
- 8. El pH de algunas sustancias piel humana: 5,5 leche: 6,5 sangre: entre 7,35 y 7,45 aproximadamente, en condiciones normales. detergente: 10,5 aproximadamente. zumo de limón: 2.
- 9. Papel tornasol El papel tornasol distingue entre ácidos y bases, es decir, toma un color cuando el pH es menor que 4.5 y toma otro color cuando el pH es mayor que 8.5. Es decir rosa y azul . Equipos para medir el pH
- 10. Papel universal El indicador universal contiene una mezcla de indicadores que permiten saber distintos rangos de pH, es decir, a diferencia del papel tornasol es un poco más específico, nos da un rango de pH para una determinada solución, poniéndose de diferentes colores cuando el pH está entre 0 -1.5, entre 1.5 y 2.5, y así siguiendo.
- 11. PH – metro El pH-metro es un sensor utilizado en el método electroquímico para medir el pH de una disolución. La determinación de pH consiste en medir el potencial que se desarrolla a través de una fina membrana de vidrio que separa dos soluciones con diferente concentración de protones. En consecuencia se conoce muy bien la sensibilidad y la selectividad de las membranas de vidrio delante el pH.
- 12. Fenolftaleína La fenolftaleína de fórmula (C20H14O4) es un indicador de pH que en soluciones ácidas permanece incoloro, pero en presencia de bases toma un color rosado o rojo grosella. Es un compuesto químico orgánico que se obtiene por reacción del fenol (C6H5OH) y el anhídrido ftálico (C8H4O3) en presencia de ácido.
- 13. Naranja de metilo rojo de metilo
- 14. Cuando en una solución la concentración de iones hidrógeno (H+)es mayor que la de iones hidroxilo (OH–), se dice que es ácida. En cambio, se llama básica o alcalina a la solución cuya concentración de iones hidrógeno es menor que la de iones hidroxilo. Una solución es neutra cuando su concentración de iones hidrógeno es igual a la de iones hidroxilo. El agua pura es neutra porque en ella [H+] = [OH–]. (Ver: Ionización del agua) La primera definición de ácido y base fue acuñada en la década de 1880 por Savane Arrhenius quien los define como sustancias que pueden donar protones (H+) o iones hidróxido (OH-), respectivamente. Esta definición es por supuesto incompleta, pues existen moléculas como el amoniaco (NH3) que carecen del grupo OH- y poseen características básicas. Teoría acido base
- 15. Tiene sabor agrio(limón, vinagre) En disolución acuosa enrojecen la tintura o papel tornasol Decoloran la fenolftaleína enrojecida por las bases Producen efervescencia con el carbonato de calcio(mármol) Neutralizan la acción de las bases Reaccionan con algunos metales como(el cinc, hierro,…), dependiendo del hidrogeno Enrojecen ciertos colorantes vegetales Disuelven sustancias Pierden sus propiedades al reaccionar con bases Los ácidos se caracterizan por:
- 16. Tiene sabor cáustico o amargo (a lejía) En disolución acuosa azulean el papel o tintura de tornasol Enrojecen la disolución alcohólica de la fenolftaleína Producen una sensación untuosa al tacto Precipitan sustancias disueltas por ácidos Neutralizan la acción de los ácidos Dan color azul a ciertos colorantes vegetales Disuelven grasas y el azufre Pierden sus propiedades al reaccionar con ácidos Las bases se caracterizan por
- 17. se hace un tampón, y los dos sistemas tampón mas populares que son los que se utilizan. se hacen añadiendo un acido débil, y su sal conjugada a una disolución. o bien una base débil y su base conjugada, dependiendo del pH al que queramos amortiguar. cualquier acido o base débil es susceptible de ser una solución amortiguadora. los dos sistemas mas conocidos son el de acido carbónico, carbonato, en la sangre, y el del acido fosfórico, fosfato, dentro de las células. Amortiguadores del PH
- 19. María Fernanda Meneses Kelly González marcela casallas Cristian camilo prieto institución Educativa fe y alegría grado :once 2013 Presentado por:
