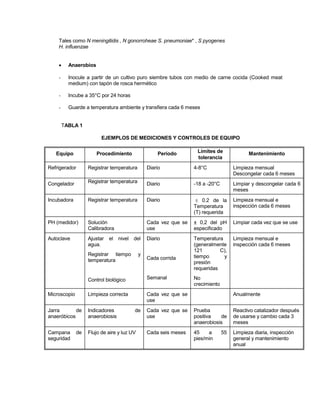
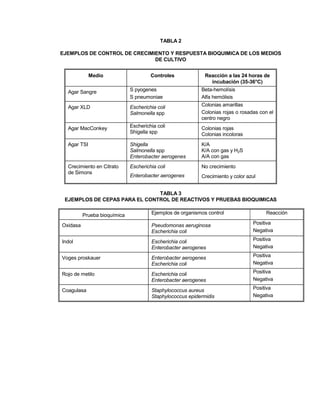
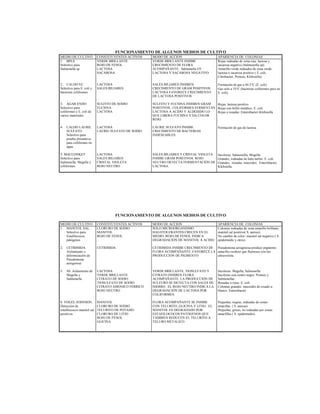
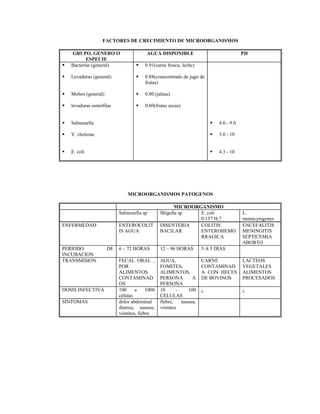
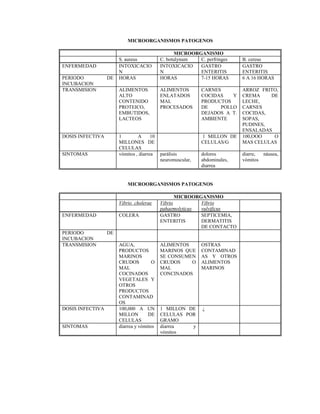
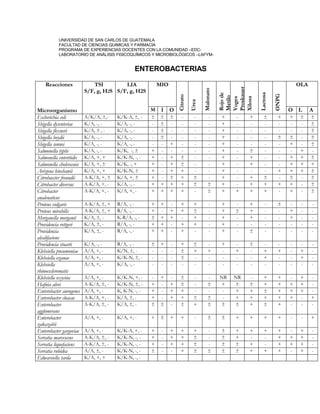
El documento trata sobre el control de calidad en los análisis microbiológicos. Explica que el control de calidad incluye monitorear diariamente los procedimientos para asegurar resultados precisos y confiables. También describe factores que influyen en la calidad como el cumplimiento de protocolos, la calibración de equipos, y el manejo adecuado de muestras, medios de cultivo e insumos. Finalmente, presenta tablas con ejemplos de cómo controlar el funcionamiento de equipos, medios de cultivo y pruebas