NEOPLASIA ENDOCRINO MÚLTIPLE [Autoguardado].pptx
- 1. NEOPLASIA ENDOCRINO MÚLTIPLE MR KEVIN CASTAÑEDA CORONEL
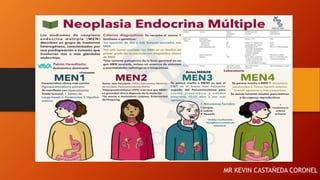
- 2. GENERALIDADES Un grupo de síndromes hereditarios que se caracteriza por crecimiento aberrante de tumores benignos o malignos en un subgrupo de tejidos endocrinos. Los tumores pueden ser funcionales o no funcionales. Hay tres síndromes principales.
- 3. MEN 1 (SD WERMER) Rasgo autosómico dominante. Prevalencia estimada de 2 a 20 por 100 000 en la población general. La edad más temprana a la cual se han reportado manifestaciones de la MEN-1 es de cinco años; la penetrancia es máxima hacia el quinto decenio de la vida.
- 4. MANIFESTACIONES CLINICAS El hiperparatiroidismo es la 1° manifestación clínica (hiperplasia 4 glándulas). Los gastrinomas, frecuentemente relacionados con síndrome de Zollinger-Ellison (ZES) de 40 a 60%. Los insulinomas constituyen 20% de los tumores de células de los islotes, y el resto tumores funcionales (p. ej., tumores productores de glucagon o de péptido intestinal vasoactivo [VIP]) y no funcionales.
- 5. GASTRINOMAS Los gastrinomas son pequeños, multicéntricos, y de ubicación ectópica fuera del lecho pancreático, más a menudo en la submucosa duodenal. A menudo son malignos. El diagnóstico hipergastrinemia en presencia de hipersecreción de ácido gástrico, prueba de estimulación de secretina.. La tomografía computarizada (CT) y la resonancia magnética (MRI) pueden ser útiles en la identificación. Las técnicas de localización comprenden ecografía endoscópica e intraoperatoria, inyección arterial selectiva de secretina (seguida por muestreo de la vena hepática para cuantificación de gastrina), y examen con octreótido radiomarcado. Como quiera que sea, es importante reconocer que casi la mitad de los gastrinomas no se encuentra con estudios de localización preoperatorios.
- 6. INSULINOMAS Los glucagonomas, VIPomas y somatostatinomas se diagnostican con base en aumentos de dos veces o más la concentración plasmática de glucagon, VIP o somatostatina, respectivamente, en presencia de uno o más nódulos pancreáticos. La ecografía endoscópica y las administraciones arteriales selectivas de calcio con muestreo de sangre de la vena hepática (para cuantificación de insulina) se han usado exitosamente para identificar lesiones en grupos pequeños de pacientes. Los insulinomas en la MEN1 se detectan usando pruebas bioquímicas convencionales. También pueden ser difíciles de localizar dado su potencial de multicentricidad.
- 7. ADENOMAS HIPOFISIARIOS • Los adenomas hipofisarios 25%. Casi todos secretan prolactina, con o sin secreción excesiva de hormona de crecimiento, seguidos hormona de crecimiento sola, tumores no funcionales, hormona adrenocorticotrópica (ACTH). • Rara vez son malignos, pero estudios recientes sugieren que pueden ser de mayor tamaño y más agresivos que sus homólogos esporádicos.
- 8. MANIFESTACIONES CLINICAS • Adenomas suprarrenales. • Se ha dicho que la enfermedad tiroidea es más común en la MEN1; • Los lipomas subcutáneos, los colagenomas de la piel, y los angiofibromas faciales múltiples se observan en 30 a 90% de los miembros de familias afectadas. • Los tumores carcinoides se observan con frecuencia aumentada en la MEN1. Son casi exclusivamente carcinoides del intestino anterior, y pueden encontrarse en el timo, en el pulmón (carcinoides bronquiales), o en la mucosa gástrica. • Los leiomiomas rara vez se han descrito en la MEN1.
- 9. MENINA PATOGENIA Se cree que el crecimiento real de un tumor requiere la inactivación somática posterior, a menudo mediante una eliminación manifiesta, de la copia normal restante del gen en una célula. Una célula paratiroidea de este tipo, por ejemplo, estaría desprovista de la función supresora de tumores normal del gen MEN1 y podría obtener una ventaja selectiva sobre sus vecinas, lo que daría como resultado una proliferación clonal.
- 10. PATOGENIA En estudios recientes se ha tenido éxito en la identificación del gen, llamado el gen menin. Menin es un producto del gen supresor tumoral. El alelo defectuoso heredado es silencioso en presencia de un alelo funcionante normal en el segundo cromosoma. Una mutación somática subsiguiente (a menudo una deleción que elimina el alelo normal) da por resultado un genotipo nulo en el cual el locus del gen supresor falta o es defectuoso en ambos alelos. Gen defectuoso al brazo largo del cromosoma 11q13. (demostrado pérdida alélica en esta área, que a menudo se produce por deleciones de DNA grandes). Autosómico dominante.
- 12. TRATAMIENTO - PARATIROIDES El hiperparatiroidismo en la MEN1 se dirige hacia la extirpación quirúrgica de tejido paratiroideo hiperplásico. En 12% persistencia (con extirpación de 3 a 3.5 glándulas paratiroides). En hasta 44% de estos casos, 8 a 12 años después de la operación se observa enfermedad recurrente, definida como reaparición de hiperparatiroidismo después de al menos tres meses de normocalcemia. La frecuencia alta de hiperparatiroidismo persistente en la MEN1 probablemente refleja la frecuencia alta de glándulas supernumerarias (prevalencia de hasta 30%) y tejido paratiroideo ectópico en pacientes que portan el gen Men1. La paratiroidectomía total se relaciona con una frecuencia más alta de hipoparatiroidismo.
- 13. TRATAMIENTO GASTRINOMA Persisten las controversias respecto a la terapia de gastrinomas en la MEN1. La supresión de la producción de ácido gástrico con inhibidores de la bomba de protones (p. ej., omeprazol) aún es una piedra angular de la terapia. El manejo médico conservador (conducta maligna de bajo grado, el fracaso de casi todos los intentos de resección quirúrgica ). Para pacientes con enfermedad metastásica hacia el hígado o hacia otros sitios, los síntomas relacionados con hipergastrinemia pueden controlarse con los antagonistas de la bomba de protones, como se describió. Los tumores de los islotes de más de 3 cm conllevan riesgo aumentado de enfermedad maligna, y por lo general se extirpan independientemente de su estado funcional.
- 14. TRATAMIENTO INSULINOMA Insulinomas rara vez están ubicados fuera del lecho pancreático. La enucleación de las lesiones identificables en la cabeza del páncreas, y la resección ciega del cuerpo y la cola del páncreas. Los pacientes no idóneos para intervención quirúrgica (pueden manejarse con terapia médica convencional (p. ej., diazóxido o verapamilo).
- 15. PRUEBAS DE DETECCIÓN Las pruebas de detección sistemáticas para mutaciones del gen Men1 no están indicadas para casos esporádicos de hiperparatiroidismo o para pacientes con tumores hipofisarios, las pruebas de detección de todos los casos de ZES probablemente tienen una buena relación costo-beneficio en la identificación de portadores. La frecuencia de mutaciones de la línea germinal en el gen Men1 en pacientes con tumores que se cree que son esporádicos con base en el análisis de la familia, es de alrededor de 5% para gastrinomas y de 1 a 2% para otras manifestaciones (p. ej., hiperparatiroidismo, prolactinomas).
- 16. PRUEBAS DE DETECCIÓN Deben limitarse a los individuos en quienes el índice de sospecha del síndrome es alta (p. ej., antecedente familiar de tumores endocrinos o estados de hipersecreción; antecedente de tumores endocrinos múltiples o afección multiglandular con hiperparatiroidismo en el caso índice). La identificación del estado de portador debe efectuarse con el fin de obtener información que permita al médico enfocar la investigación en la población de pacientes relevante. No debe usarse para apoyar una intervención terapéutica mayor. Esas intervenciones (p. ej., exploración del páncreas) pueden relacionarse con morbilidad importante, y no hay evidencia de que prolonguen la supervivencia del paciente. Hiperparatiroidismo deben investigarse para MEN1 — incluso en ausencia de un antecedente familiar o de cualquier antecedente de tumores endocrinos múltiples— si se identifica hiperplasia paratiroidea en el momento de paratiroidectomía, o si hay un antecedente de hiperparatiroidismo recurrente después de paratiroidectomía. Los pacientes con ZES deben investigarse para MEN1 dada su frecuencia alta (∼25%) en esos individuos. Los pacientes con lesiones aisladas tienen una probabilidad baja de tener MEN1 coexistente, y probablemente no requieren pruebas de detección a menos que haya otros datos clínicos que sugieran el síndrome.
- 17. PRUEBAS DE DETECCIÓN La penetrancia de la MEN1 es de más de 95% hacia los 45 años de edad. Las pruebas de detección deben continuarse a intervalos periódicos al menos hasta esa edad; si para entonces no hay evidencia de afección de órgano endocrino típica, podría reducirse la frecuencia de las pruebas de detección. Sin embargo, tiene importancia notar que el riesgo no se reduce a cero a los 45 años de edad. Una minoría de los pacientes se presenta con su primera manifestación del síndrome bastante después de los 45 años de edad. La resección quirúrgica de tejido enfermo (p. ej., paratiroidectomía) debe ir seguida por pruebas de detección continuas para buscar tanto enfermedad recurrente como afección de otros órganos.
- 19. NEOPLASIA ENDOCRINA MÚLTIPLE TIPO 2 (SD SIPPLE) • Autosómico dominante. • Prevalencia de 1 a 10 por 100 000 en la población general. • Subdivide: MEN 2A con Enf. Hirschsprung / liquen amiloide/ Ca tiroides medular familiar. • MEN2B (MEN 3) • La penetrancia de la MEN 2 es de más de 80% en individuos que portan el gen defectuoso.
- 20. MANIFESTACIONES CLINICAS • El carcinoma medular de la tiroides es la manifestación más común y a menudo la primera presentación clínica. • De los individuos en riesgo, 80 a 100% presenta MCT en algún momento de su vida. • La lesión tiroidea clásica de la MEN2 es la hiperplasia de las células parafoliculares productoras de calcitonina, que típicamente es el precursor de MCT. Estos tumores en pacientes con MEN2 tienden a ser multicéntricos y a estar concentrados en el tercio superior de la glándula tiroides, lo que refleja la distribución normal de las células parafoliculares.
- 21. Patogenia Cromosoma 10. Gen defectuoso estaba estrechamente enlazado al protooncogén ret. La RET es una proteína enlazada tirosina cinasa, de dominio transmembrana único, que forma parte del receptor de factor neurotrófico derivado de la línea de células gliales (GDNF). Este receptor, el GDNFR (receptor del factor neurotrófico derivado de línea de células gliales), es una proteína de superficie celular enlazada a glucosil fosfatidil inositol. Se ha mostrado que otros ligandos, la neurturina, persefina y artemina, se relacionan con RET y lo activan mediante sus receptores cognados GDNFRα1-4. Se cree que estos residuos cisteína ejercen un control inhibidor tónico sobre la actividad de RET en la célula normal.
- 22. PATOGENIA el protooncogén reordenado durante la transfección (RET) es un receptor de glicoproteína transmembrana con actividad tirosina quinasa que transduce señales de crecimiento y diferenciación en varios tejidos en desarrollo, incluidos los derivados de la cresta neural. Las variantes patógenas de la línea germinal en RET que dan como resultado una ganancia de función causan MEN2, mientras que las mutaciones somáticas de RET se asocian con cánceres medulares de tiroides esporádicos.
- 24. PRUEBAS DE DETECCIÓN Pruebas basadas en reacción en cadena de polimerasa (PCR) diseñadas para identificar mutaciones específicas en la secuencia codificadora RET. Las pruebas genéticas para mutaciones de la línea germinal de RET probablemente están indicadas para todos los pacientes que se presentan con MCT. Se recomiende tiroidectomía total en todos los individuos que albergan una mutación de RET relacionada con MEN2. deficiencias relativas de las pruebas bioquímicas en contraposición con las genéticas.
- 26. TRATAMIENTO El tratamiento de MCT heredables debe incluir tiroidectomía total con al menos disección de los ganglios linfáticos centrales. Dada la naturaleza multicéntrica de la enfermedad, la tiroidectomía subtotal no se recomienda. Las concentraciones de calcitonina basales o estimuladas se usan en la situación posoperatoria para evaluar la presencia de enfermedad residual. El tratamiento de feocromocitomas en la MEN2 es similar al que se utiliza para feocromocitomas esporádicos.
- 27. MEN 4 • MUTACIÓN GEN CDKN1B EN EL CROMOSOMA 12P13: DESCRITO 20 CASOS INDICE. • MISMAS CARACTERISTICAS CLINICAS DEL MEN1.
Notas del editor
- Los tumores no funcionales típicamente se diagnostican después de estudios de imágenes luego de exclusión
- Tiene importancia recordar que el calcio estimula la secreción de ácido gástrico. Esto puede ocurrir por medio de vías dependientes de gastrina e independientes de. En pacientes con MEN1 que presentan tanto hiperparatiroidismo como ZES, la corrección del hiperparatiroidismo y de la hipercalcemia acompañante suele dar lugar a una reducción de la producción de ácido tanto basal como máxima, y una declinación de la concentración sérica de gastrina. Las pruebas de estimulación de secretina a menudo se normalizan después de paratiroidectomía. Lo que es más importante, después de intervención quirúrgica paratiroidea, la dosis de medicamento (p. ej., inhibidor de la bomba de protones) requerida para controlar los síntomas de ZES se reduce en alrededor de 60% de los pacientes.
- Típicamente, esto es antes de los seis meses de edad en la MEN2B y antes de los cinco años de edad en la MEN 2A.
