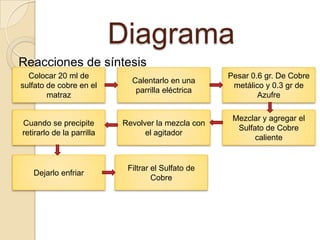
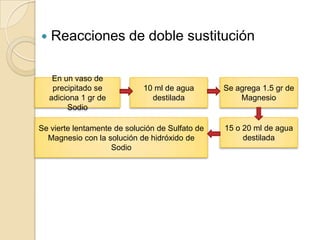
Este documento describe tres tipos de reacciones químicas: reacciones de síntesis, reacciones de descomposición y reacciones de doble sustitución. Incluye instrucciones para realizar experimentos que ilustran cada tipo de reacción, así como preguntas sobre la toxicidad de los reactivos y ejemplos adicionales de reacciones.