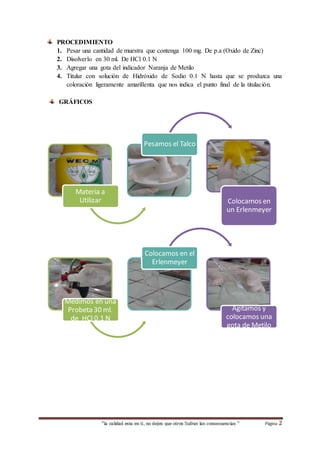
Este documento presenta los resultados de un análisis de control de calidad realizado a una muestra de talco con óxido de zinc. Se determinó que la concentración de óxido de zinc en la muestra fue de 105.63%, cumpliendo con los parámetros de referencia establecidos entre 90-110%. El objetivo de realizar esta prueba era verificar que la cantidad de principio activo en el producto era la correcta.