Este documento describe una práctica de laboratorio realizada para estudiar la intoxicación por cobre en pollos. La práctica involucró la administración de sulfato de cobre a un pollo, la disección y destilación de sus vísceras, y la realización de varias pruebas químicas que confirmaron positivamente la presencia de cobre a través de precipitados de colores característicos. El objetivo era observar los efectos de la intoxicación por cobre y aprender a identificarlo en muestras biológicas.




![5
“Todo es veneno nada es veneno todo depende de su dosis”
(NO3)Cu + 2CNNa (CN)2Cu + NO3- + Na+
(NO3)Cu + 3CNNa [Cu(CN)3]= + 3Na+
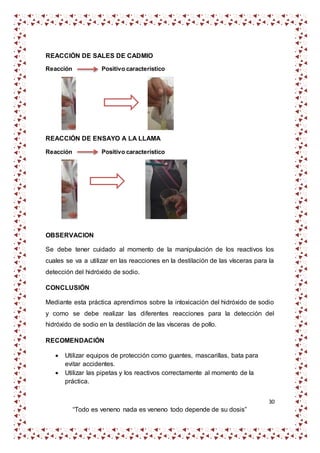
Con el Hidróxido de Amonio: A la solución muestra, agregarle algunas gotas
de NH4OH, con lo cual en caso positivo se forma un precipitado color
azul claro de solución NO3 (OH) Cu. Este precipitado es soluble en exceso de
reactivo, produciendo solución color azul intenso que corresponde al complejo
[Cu(NH3)4]++.
(NO3)2Cu + NH3 Cu(OH)NO3
(NO3)2Cu +3 NH3 2[Cu(NH3)4+++ NO3H + H2O
Con el Hidróxido de Sodio: A 1ml de solución muestra, agregamos algunas
gotas de NaOH, con lo cual en caso de ser positivo se debe formar un
precipitado color azul pegajoso por formación de Cu (OH)2. Este precipitado es
soluble en ácidos minerales y en álcalis concentrados.
Cu++ + 2OH Cu(OH)2Con el SH2:
Con el SH2: A la solución muestra, hacerle pasar una buena corriente de SH2,
con lo cual en caso de ser positivo se forma un precipitado color negro este
precipitado es insoluble en exceso de reactivo, en KOH 6M, en ácidos
minerales diluidos y fríos.
(NO3)2Cu + SH2 SCu+ 2NO3H
Con el IK: A una pequeña porción de solución muestra agregarle gota a gota
de solución de IK, con lo cual en caso de ser positivo se forma inicialmente un
precipitado color blanco que luego se transforma en pardo verdoso o por
formaciones de iones tri yoduros, el mismo que se puede volar con Tío sulfato
de sodio.
(NO3)Cu + Tri yoduros
GRAFICO
Escoger el animal
de experimentación
Aplicando el toxico
Observamos los síntomas
que presenta el pollo](https://image.slidesharecdn.com/practicas-170906221805/85/Practicas-5-320.jpg)



























![34
“Todo es veneno nada es veneno todo depende de su dosis”
Vasos de precipitación
Agitador
Cable de electricidad
2 focos
Interruptor
Mandil
Recipiente de vidrio
Llave
Cuchara
Moneda
Pinzas (forma de lagarto)
Cinta
EQUIPO
Equipo de carga iónicas
SUSTANCIAS
Agua destilada
Cianuro
MUESTRA
Alimento de experimentación
(yuca)
ACTIVIDADES A REALIZAR
Limpiar el mesón de trabajo y tener a mano todos los materiales a
utilizarse.
Preparar la conexión de electricidad.
Colocando la yuca en la campana, y observar en qué estado se
encuentra.
Colocar un pedazo de yuca en un recipiente de vidrio para la
determinación cuantitativa de CN‾ en la planta mediante la
comprobación de cada estudiante tocando para ver que haya presencia
de electricidad.
REACCIÓN DE IDENTIFICACIÓN
METODO DE DENIGES
Constituye una valoración en donde se forma una sal de AgCN y el exceso de
Ag en el punto final forma un compuesto de color amarillo con el ion ioduro de
acuerdo con las siguientes reacciones:
CN‾ + Ag NO₃ AgCN + NO₃
AgCN + CN -[Ag (CN)₂] – (Complejo soluble)
[Ag (CN)₂] +Ag +Ag (CN)₂ Ag (se forma antes de pto. Final)
Se corrige con NH₃
Ag (CN)₂ + NH₃ Ag (NH₃)₂
Ag + exceso + I – AgI amarillo](https://image.slidesharecdn.com/practicas-170906221805/85/Practicas-34-320.jpg)

