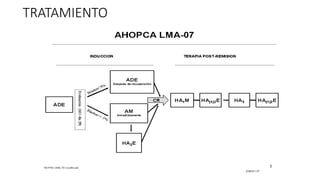
Este protocolo tiene como objetivos mejorar la sobrevida libre de enfermedad a 5 años al menos en un 40% en pacientes menores de 18 años con leucemia mieloide aguda no promielocítica, y evaluar la respuesta completa, sobrevida libre de eventos, sobrevida libre de enfermedad y sobrevida global. El tratamiento consiste en inducción con quimioterapia, tratamiento del sistema nervioso central, terapia post-remisión y estudios durante y después del tratamiento.