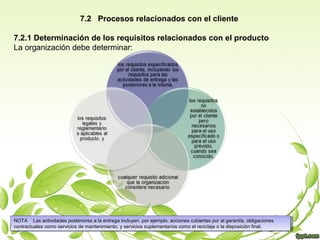
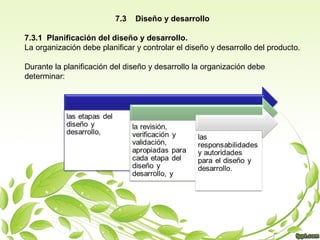
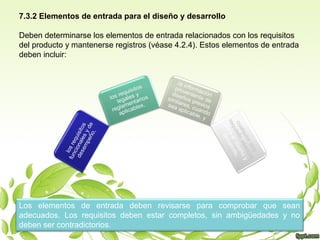
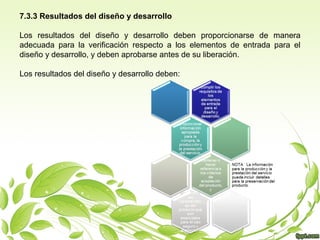
Este documento describe los procesos requeridos para la realización del producto. Estos incluyen planificar y desarrollar los procesos de producción, determinar y revisar los requisitos del cliente, diseñar y desarrollar el producto, realizar compras, controlar la producción y la prestación de servicios, e identificar y hacer un seguimiento del producto. El objetivo es asegurar que se cumplan los requisitos del cliente y los estándares de calidad en todas las etapas del proceso de producción.