Trabajo de quimica
•Descargar como PPTX, PDF•
0 recomendaciones•66 vistas
Mapa Conceptual de Quimica I
Denunciar
Compartir
Denunciar
Compartir
Recomendados
Recomendados
Más contenido relacionado
La actualidad más candente
La actualidad más candente (20)
Último
Último (20)
El Futuro de la Educacion Digital JS1 Ccesa007.pdf

El Futuro de la Educacion Digital JS1 Ccesa007.pdf
El liderazgo en la empresa sostenible, introducción, definición y ejemplo.

El liderazgo en la empresa sostenible, introducción, definición y ejemplo.
tema 6 2eso 2024. Ciencias Sociales. El final de la Edad Media en la Penínsul...

tema 6 2eso 2024. Ciencias Sociales. El final de la Edad Media en la Penínsul...
Evaluación de los Factores Externos de la Organización.

Evaluación de los Factores Externos de la Organización.
Proyecto de Participación Estudiantil Completo - Bachillerato Ecuador

Proyecto de Participación Estudiantil Completo - Bachillerato Ecuador
Pasos para enviar una tarea en SIANET - sólo estudiantes.pdf

Pasos para enviar una tarea en SIANET - sólo estudiantes.pdf
Diseño Universal de Aprendizaje en Nuevos Escenarios JS2 Ccesa007.pdf

Diseño Universal de Aprendizaje en Nuevos Escenarios JS2 Ccesa007.pdf
FICHA DE LA VIRGEN DE FÁTIMA.pdf educación religiosa primaria de menores

FICHA DE LA VIRGEN DE FÁTIMA.pdf educación religiosa primaria de menores
ACERTIJO CÁLCULOS MATEMÁGICOS EN LA CARRERA OLÍMPICA. Por JAVIER SOLIS NOYOLA

ACERTIJO CÁLCULOS MATEMÁGICOS EN LA CARRERA OLÍMPICA. Por JAVIER SOLIS NOYOLA
Santa Criz de Eslava, la más monumental de las ciudades romanas de Navarra

Santa Criz de Eslava, la más monumental de las ciudades romanas de Navarra
Síndrome piramidal 2024 según alvarez, farrera y wuani

Síndrome piramidal 2024 según alvarez, farrera y wuani
Gran Final Campeonato Nacional Escolar Liga Las Torres 2017.pdf

Gran Final Campeonato Nacional Escolar Liga Las Torres 2017.pdf
Trabajo de quimica
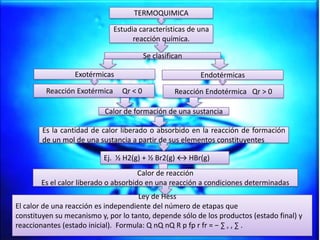
- 1. TERMOQUIMICA Estudia características de una reacción química. Se clasifican Exotérmicas Reacción Exotérmica Endotérmicas Qr < 0 Reacción Endotérmica Qr > 0 Calor de formación de una sustancia Es la cantidad de calor liberado o absorbido en la reacción de formación de un mol de una sustancia a partir de sus elementos constituyentes Ej. ½ H2(g) + ½ Br2(g) ↔ HBr(g) Calor de reacción Es el calor liberado o absorbido en una reacción a condiciones determinadas Ley de Hess El calor de una reacción es independiente del número de etapas que constituyen su mecanismo y, por lo tanto, depende sólo de los productos (estado final) y reaccionantes (estado inicial). Formula: Q nQ nQ R p fp r fr = − ∑ , , ∑ .